
24.(10)KMnO4溶液常用做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此精确配制KMnO4标准溶液的操作是:
(1)称取稍多于所需量的KMnO4固体溶于水,将溶液加热并保持微沸l h;
(2)用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;
(3)过滤得到的KMnO4溶液贮存于棕色试剂瓶放在暗处:
(4)利用氧化还原滴定方法,在
回答下列问题:
(1)为什么要称取稍多于所需的KMnO4固体?___________________________
(2)如何保证在70℃~
(3)下列物质中,可以用于测定KMnO4溶液浓度的基准试剂是________(填写序号)
A.H
 ②根据反应①与②推导出Q1、Q2、Q3的关系式Q3=_____________;
②根据反应①与②推导出Q1、Q2、Q3的关系式Q3=_____________;
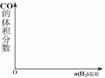
(3)现在恒容密闭容器中通入一定量CO2,再慢慢通入H2,使发生
上述反应③,在其他条件不变时,若改变H2的起始量,容器中
CO的体积分数也随之改变,使在右图中画出CO的体积分数随
n(H2)变化的示意图。
(2)现有反应③H2(g)+CO2(g)  CO(g)+H2O(g)
△H=Q3
CO(g)+H2O(g)
△H=Q3
①根据反应①与②推导出K1、K2、K3的关系式K3=_____________;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有__________________。
A.缩小容器体积 B.降低温度
C.使用合适的催化剂 D.设法减少CO的量 E.升高温度
1.67
(1)从上表可推断,反应①是________(填“放”或“吸”)热反应;
2.15
2.38
1173
1.47
23.(10分) 设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) △H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) △H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)  FeO(s)+H2(g) △H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) △H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
T/K
K1
973
 |
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O。
②ClO2的沸点为283K,纯ClO2易分解爆炸,常用稀有气体或空气稀释防止爆炸性分解
③HClO2在25℃时的电离常数与硫酸的第二步电离常数相当,可视为强酸。
(1)160g/LNaOH溶液的物质的量浓度为 。若要计算该溶液的质量分数,还需要的一个数据是 。
(2)ClO2发生器中所发生反应的化学方程式为 。
(3)吸收塔中为防止产生NaClO2被继续还原成NaCl,所用还原剂的还原性应适中。除H2O2处,还可以选择的还原剂是 (填序号)
A、Na2O2 B、Na2S C、FeCl2 D、KMnO4
(4)从滤液中得到NaClO2?3H2O晶体还必须进行的操作是 (填操作名称)
22. (9分)亚氯酸钠(NaClO2)是一种重要的含氯消毒剂。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com