
87.5
76.0
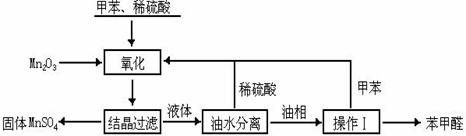
试回答下列问题:
⑴Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是______________。
⑵甲苯经氧化后得到的混合物通过结晶、过滤进行分离。该过程中需将混合物冷却,其目的是______________。
⑶实验过程中,可循环使用的物质分别为_______、_______。
⑷实验中分离甲苯和苯甲醛采用的操作Ⅰ是______________,其原理是______________。
⑸实验中发现,反应时间不同苯甲醛的产率也不同(数据见下表)。
反应时间/h
1
2
3
4
5
苯甲醛产率/%
27.(10分)苯甲醛在医药、染料、香料等行业有着广泛的应用。实验室通过下图所示的流程由甲苯氧化制备苯甲醛。
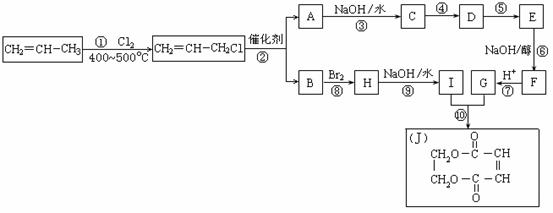
请按要求填空:
(1)写出下列反应的反应类型:①:__________,⑥:___________,⑧:______________。(2)反应②的化学方程式是___________________________________________。
(3)反应④、⑤中有一反应是与HCl加成,该反应是________(填反应编号),设计这一
步反应的目的是_____________ ________,物质E的结构简式是____________________。
(4)反应⑩的化学方程式是___________________________________________。
六、(选做题,本题共10分)

现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。
26.(10分)2005年的诺贝尔化学奖颁给了3位在烯烃复分解反应研究方面做出突出贡献的化学家。烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应。如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子――丁烯和乙烯。
(3)某化验室称取0.5000g矿石样品按上述过程进行成分分析,在滴定过程中消耗了22.50mL0.1000mol/L的H
25.(8分)金属钒(V)在材料科学上有重要作用,被称为“合金的维生素”。以下是测定矿石中钒的含量的两个反应:
(1)用稀硫酸溶解五氧化二钒,得到(VO2)2SO4溶液。写出该反应的化学方程式
_________________________________________________________________。
(2)用已知浓度的硫酸酸化的H
VO2+ + H
a.VO2+和Cl2氧化性的相对大小 b.VO2+和HCl氧化性的相对大小
(4)若准确称取W g草酸晶体(H
6H++2MnO4-+5H
①滴定时,高锰酸钾溶液应装在________________;
②滴定终点标志是__________________;
③KMnO4溶液的物质的量浓度为__________________:
④若滴定前平视,滴定后俯视,则测得的浓度值将________(填“偏高”或偏低)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com