
2、(8分)
2005年5月22日,中国登山测量队成功登上珠峰顶,圆满完成珠峰高度最新测量工作。登山队员常用的能源是氢化钙(CaH2)固体,用它和水反应生成氢气供燃烧之需,化学方程式为:CaH2+2H2O=Ca(OH)2+2H2↑,请回答下列问题:
(1)CaH2中钙元素为+2价,氢元素的化合价为 。
(2)现有875g CaH2固体,与足量水反应可生成多少克氢气?
1、(6分)
某地一不法商贩销售的“尿素”中,经检验含氮的质量分数为28%。
求:(1)已知尿素的化学式为CO(NH2)2,则尿素中氮元素的质量分数是多少?
(2)该商贩所售每袋“尿素”(50kg),实际含尿素多少千克?
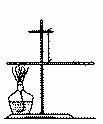
(1)冷却后,他们观察到的现象是:①______________,②_________________________。
(2)写出铜丝加热时所发生的化学方程式:______________________。
3、(4分)
某兴趣小组为了探究质量守恒定律,进行了如右图所示的小实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上40cm长的粗铜线,并使玻璃棒保持水平,然后,用酒精灯给左边一端铜丝加热1~2分钟。停止加热后冷却,仔细观察发生的现象。
④待步骤③的试管中没有气泡后,进行“某一操作”将固体洗净、干燥、称量,得红色固体的质量仍为0.5g
[现象]甲同学观察到步骤①中的现象为_________________,步骤③中带火星的木条复燃。
[反思]步骤④中进行的“某一操作”是_________________,
乙同学认为在步骤④后还需增加一个实验,请你写出该实验的操作方法和现象__________________________________________________。
[结论]通过以上步骤得出的结论是_________________________________________________请你举出一生活中应用催化剂的事例__________________________________
②用精密的天平准确称量0.5g Fe2O3红色粉末,并将其加入另一试管中
③在步骤②的试管中加入5mL5%的H2O2溶液,把带火星的木条伸入试管
[猜想]甲同学认为CuO或Fe2O3可以代替MnO2,因为按物质的分类MnO2、CuO、Fe2O3都属于
[设计实验]甲同学按下面步骤进行实验:
①在试管中加入5mL5%的过氧化氢溶液,把带火星的木条伸入试管
2、(7分)
催化剂在生产、生活和科研中有重要作用,实验用过氧化氢分解制氧气,常用MnO2作催化剂。
[提出问题]其他物质能作过氧化氢的催化剂吗?
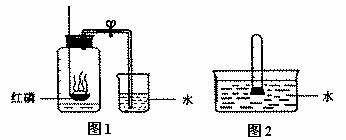
(1)写出磷燃烧的化学方程式:__________________
(2)实验2中,在水中而不在空气中取下橡皮塞的原因是_____________________________
(3)从测定结果分析,上述实验中效果较好的实验是________,
写出另一个实验的两点不足________________________
1、(5分)
下面是测定空气中氧气体积含量的两个实验:
实验1:在集气瓶内预先装少量水,余下的容积5等分,做好标记。在带橡皮塞和导管的燃烧匙内装足量的红磷,立即伸入集气瓶内塞紧橡皮塞(如图1所示),待红磷熄灭并冷却到室温后打开弹簧夹。
实验2:将试管的容积5等分,做好标记,在试管中加入一小块白磷(足量),用橡皮塞塞紧试管口,将试管放入热水中使白磷燃烧,待白磷熄灭并冷却到室温后,将试管倒立于盛有室温下水的水槽中(如图2所示),并在水中将橡皮塞取下。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com