
23、(4分)有A、B、C、D、E、F六种物质的稀
溶液,已知它们分别是K2CO3、BaCl2、Ca(NO3)2、NaCl、H2SO4、AgNO3中的某一种溶液。
22、(8分)芒硝(Na2SO4•10H2O)是一种重要的化工原料,具有广泛的用途。
(1)在我国广西某地区一大型芒硝矿。从广西的地理和气候环境推测,该大型芒硝矿床应存在于地层深处,原因是 。
(2)为测定Na2SO4和NaCl混合物样品中Na2SO4的质量分数,甲、乙两位同学按下列步骤进行实验:称量样品,加水溶解后加过量的试剂A。过滤除沉淀,烘干,称量,处理实验数据并得出结果。
a 对实验的试剂A,甲同学选用硝酸银溶液,而乙同学悬挂用氯化钡溶液。其中一位同学选用的试剂不合理,请说明不合理的原因 。
b 若试剂A选择正确,在进行实验时:
①检验加入的试剂A是否已过量的方法是 。
②入食盐中测的样品质量Wg,沉淀物质量为mg,则样品中Na2SO4的质量分数为 (填结果既可)
21、(2分)在一在已调平的天平的两盘上,各方以盛有质量和质量分数相等的稀盐酸的烧杯,向左盘烧杯中加入
4.5
178
97
35
11
494
(2)根据曲线讨论溶液温度变化的原因。
①加入盐酸的量在2-10mL之间时: ;
②加入盐酸的量在lO-20mL之间时: 。
(3)若某同学提出“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,此提议是否合理?为什么?
答: 。
20(4分)下表列出了
H2
NO2
CO2
O2
N2
Cl2
气体沸点/℃
-252
-33
-78
-183
-196
-34
吸附气体体积/mL
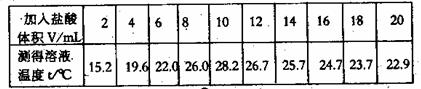
(1)试绘出溶液的温度与加入盐酸的体积之间的变化关系曲线。
18、(4)高纯度的单质硅是信息产业的核心资料,没有硅,就没有你喜欢的计算机。在地壳中含有大量的硅元素,含量仅次于氧,但自然界中没有游离的硅,硅元素全部是以化合态的形式存在的,石英砂的主要成分就是二氧化硅。运用你学过的有关知识回答下列问题:
(1)在工业上,可用碳在高温下还原二氧化硅制得含少量杂质的粗硅,该反应属于置换反应,反应的产物之一是一氧化碳。则该反应的化学方程式为 。
(2)以粗硅为原料,制备高纯硅的一种方法为①用镁和粗硅反应得到硅化镁(Mg2Si);②将硅化镁与盐酸反应得到硅烷(SiH4)和一种盐;③加热硅烷得到高纯硅和另一种气体单质。
反应②的化学反应方程式为 。
反应③的化学反应方程式为 。
19(5分)在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸,反应中溶液的温度与加入盐酸的体积变化如下:
17、(3分)铁路提速为鲜活水产品、新鲜水果和蔬菜的运输提供了有利条件。在鲜活鱼的长途运输中,必须考虑以下几点:水中需要保持适量的O2;及时除去鱼排出的CO2;防止细菌的大量繁殖。现有两种在水中能起供氧灭菌作用的物质是,其性质如下:
过氧化南(Na2O2):易溶于水,与水反应生成NaOH和O2;
过氧化钙(CaO2):微溶于水,与水反应生成Ca(OH)2和O2。
根据以上介绍,你认为运输鲜活水产品时选择 加入水中更好?因为 。
16、下列观点不正确的是
A 为提高粮食产量,应提倡大量施用化肥和农药
B 绿色植物的光合作用将光能转化为化学能
C大自然中不断进行着物质的妆化和能量转化,太阳能在转化过程中起到了至关重要的作用
D 通过化学反应可以发电
15、将少许食盐投入到一杯水中,食盐逐渐溶解,水变咸了;若将水温提高,再投入食盐,实验能继续溶解,且溶解速度加快。仅仅通过上述现象,我们无法得出的结论是( )
A 微观粒子间是有间距的 B 温度升高,固体物质的溶解度一定增大
C 微观粒子是不断运动的 D 温度升高,微观粒子运动加快
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com