
32、通常状况下,人体呼出气体中部分气体的含量和空气中部分气体的含量如下表所示。(含量指各组分的体积分数)
.
空气中的含量(%)
呼出 气体中的含量
氧气
21
结论(2х0.5分)
猜想(2х0.5分)
实验操作
实验现象
31、碳酸铵[化学式(NH4)2CO3]可用作氮肥。在试管中加热碳酸铵能生成三种化合物,
其中一种是氨气(化学式:NH3)。请你根据所学知识。猜想另外两种生成物各是什么物质,并设计实验证明你的猜想(将有关内容填在下表中)。
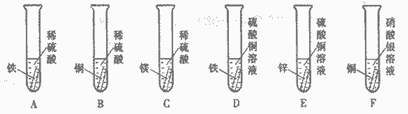
(1)上述实验中,有气泡产生的是(填写装置序号)
(2)F中出现的现象是 __________
(3)通过上述实验,能否证明镁、锌、铁、铜、银五种金属的活动顺序?并说明理由。_____________________________________________________________________
30、如图3所示,某同学探究金属化学性质的实验。
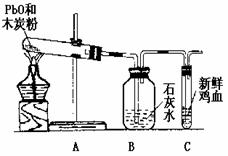 29、小强、小明和小梅三同学在学习了木炭还原氧化铜的实验后,提出如下问题:“木炭与一氧化铅(化学式为PbO)反应生成铅的同时产生的气体一定全部为二氧化碳吗?”请你和他们一起对产物中气体的成分进行研究,并回答有关问题。
29、小强、小明和小梅三同学在学习了木炭还原氧化铜的实验后,提出如下问题:“木炭与一氧化铅(化学式为PbO)反应生成铅的同时产生的气体一定全部为二氧化碳吗?”请你和他们一起对产物中气体的成分进行研究,并回答有关问题。
(1)猜想:小强认为:反应产生的气体全部
为二氧化碳。小明认为:反应产生的气体
全部为一氧化碳。小梅认为:反应产生的
气体既有二氧化碳又有一氧化碳。
(2)设计实验:根据各自的猜想,他们共同设计了实验,实验装置如右图(他们在实验
中进行了规范操作和细致的观察)。
(3)现象与结论:如果小强猜想正确,装置B、C中的实验现象是
;如果小明猜想正确,装置B、C中的实验现象是
。如果小梅猜想正确,装置B、C中的实验现象是
(4)此实验装置有不足之处,请你对该装置进行改进,具体措施是
。
(5)根据上述实验及学习的木炭与CuO、Fe2O3的反应,请你归纳出单质碳的一项重要用途是 。
28、(1)市场上销售的香肠、盐水鸭、榨菜、豆腐干等食品,常采用真空包装。真空包装的目的是除去空气,使大多数微生物因缺少 气而受到抑制,停止繁殖,同时防止食品发生缓慢 而变质。
(2)茶叶、肉松、膨化食品等常采用真空充气包装,即将食品装入包装袋,抽出包装袋内空气,再充人防止食品变质的气体,然后封口。真空充气包装能使食品保持原有的色、香、味及营养价值,防止食品受压而破碎变形。
【提出问题】充入食品包装袋中的气体是什么?
【猜想与验证】
可能是N2。实验初步验证的方法及现象:
充人的气体还可能是:① ;②
27、若取质量均为mg镁和铁,分别投入到
①充分反应后,一定有剩余的金属是_____
②m的取值范围为____________,反应中消耗掉金属镁的质量为____________
③硫酸中H2SO4质量分数为_______
26、某课外兴趣小组,确立了“酸碱中和生成的正盐溶液的性质”作为研究课题,在研究
中他们发现,正盐虽然不能电离出氢离子或氢氧根离子,但是其溶液却不一定呈中性,
有的呈酸性,有的呈碱性。为什么呢?盐溶液的酸碱性与什么有关呢?由“组成、结构
决定物质性质”的观点出发,他们又进一步从组成特征上去找原因, 发现正盐溶液的酸
碱性与对应的酸和碱的强弱有关。他们将实验结果统计如下:
酸
碱
相应的正盐
溶液的pH
HCl (强酸)
NaOH (强碱)
NaCl
7
H2SO4(强酸)
KOH (强碱)
K2SO4
7
H2CO3(弱酸)
NaOH (强碱)
Na2CO3
> 7
H3PO4(弱酸)
KOH (强碱)
K3PO4
> 7
HNO3 (强酸)
Cu(OH)2 (弱碱)
Cu(NO3)2
< 7
HCl (强酸)
Fe(OH)3 (弱碱)
FeCl3
< 7
⑴请你根据上表归纳出正盐溶液的酸碱性与对应酸、碱的强弱关系:(至少写2条)
⑵根据他们的发现,请你判断硝酸钠、硝酸铁、硫酸铜、氯化钾、磷酸钠、碳酸钾六种溶液的酸碱性,其中溶液呈酸性的是 _________、呈碱性的是 、呈中性的是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com