
(1)在上述溶液中加入质量分数为3.65%的盐酸,若充分反应后,溶液呈中性。加入盐酸的质量是多少?
(2)计算原混合物中Na2O和Na2O2的质量。
16.(5分)已知Na2O2是一种淡黄色粉末,易与水反应,生成氢氧化钠和一种能使带火星的木条复燃的气体。现有Na2O和Na2O2的混合物
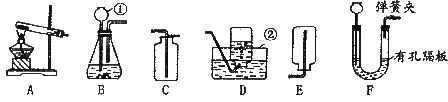
(1)写出标号①②的仪器名称:① ②
(2)实验室用Zn与稀H2SO4制取H2,可选用装置 (填写装置序号)能收集到较纯净的H2。
(3)用高锰酸钾制取O2,装置A还需做的一点改动是 。
(4)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过以下
四步实验操作可回收二氧化锰。正确操作的先后顺序是 。(填写选项序号)
A.烘干 B.溶解 C.过滤 D.洗涤
(5)把(4)中滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是
。(6)用装置F制取气体,在反应过程中,用弹簧夹夹住导气管上的橡皮管,过一会儿反应就会停止。其原因是 。
15.请根据下图装置,回答问题:
14.(4分)实验探究:氢氧化钠溶液中哪一种粒子(H2O、Na+、OH-)能使指示剂变色。
实验步骤:
(1)在第一支试管中加入约2 mL蒸馏水,滴人几滴无色酚酞试液,观察现象;
(2)在第二支试管中加入约2 mL NaCl(pH=7)溶液,滴入几滴酚酞试液,观察现象;
(3)在第三支试管中加入约2 mL NaOH溶液,滴入几滴无色酚酞试液,观察现象;
通过上述实验的探究,回答下列问题(下述“现象”是指:无色酚酞试液是否变红):
实验(1)你得出的结论是: ;
实验(2)说明Na+离子 ;
实验(3)看到的现象是 ;你得出的结论是: 。
(3)三变:若用
(2) 二变:若用
13.(4分)锌与盐酸反应可制得氢气,另一产物为氯化锌,试写出反应的化学方程式
。
(1)一变:若用A+B→AB表示化合反应。AB→A+B,表示分解反应,则上述反应可表示为 。
12.(2分)中考前,枣庄市对初中毕业生进行化学实验操作考核,小翔抽到的题签是:检验溶液的酸碱性。他选择紫色石蕊试液完成了这个实验。一直喜欢科学探究的他在得知成绩合格后,立即向老师询问,知道了样品1是稀NaCl溶液,样品2是稀HCl溶液,样品3是稀Na2CO3溶液。细心的小翔还发现自己的废液缸里的废液显红色;请你帮助小翔分析:
(1)废液里一定含有的物质是 (石蕊试液和水不填)。
(2)废液呈红色的原因可能是 。
(3)若生成的气体中碳元素与氧元素的质量比介于3:8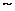 3:4之间,则生成物为 。
3:4之间,则生成物为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com