
2.正确的实验操作是获得正确的实验结果和保障人身安全的前提下图所示的实验操作正确的是( )
C.该元素在地壳中的含量为52.00%
D.该元素的原子核外有24个电子
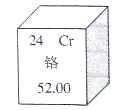
A.该元素的原子序数为52
B.该元素属于非金属元素
1.元素周期表是学习化学的重要工具,下图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )
24.(8分)我市北临渤海湾,是全国重要的产盐区。下图是某盐场生产并处理过的工业盐产品质量指标。某学习小组为了测定该工业盐中氯化钠的质量分数,进行如下实验:①取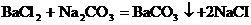 l)。求:
l)。求:
(1)
(2)通过计算,判断该工业盐中氯化钠的质量分数是否符合产品质量指标。(计算结果保留2位小数)
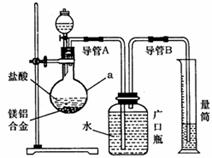
(1)研究小组利用上图所示实验装置,按照方案1进行了实验。
①装置中仪器a的名称是 。
②实验装置中有一处明显错误,请指出
(2)方案2中剩余固体是 ;若按方案2进行实验,测得镁的质量分数为 。
(3)方案3中“过滤”得到的沉淀是 。
(4)某同学又设计了与上述方案原理不同的方案4,也能测得镁的质量分数。请你在横线上填写合适的内容,将该方案补充完整。
方案4:镁铝合金与
反应测定生成气体在标准状况下的体积为V
【方案评价】
(5)在实验方案1―4中,你认为最佳的实验方案是 。
五、计算题(本题包括l小题。共8分)
【查阅资料】已知铝与NaOH溶液反应生成易溶于水的偏铝酸钠(NaAlO2:)和H2,化学方程式为: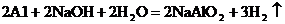 ;镁不与NaOH溶液反应。氢氧化铝能与氢氧化钠溶液发生反应生成易溶于水的偏铝酸钠(NaAlO2:)和H2O,化学方程式为:
;镁不与NaOH溶液反应。氢氧化铝能与氢氧化钠溶液发生反应生成易溶于水的偏铝酸钠(NaAlO2:)和H2O,化学方程式为: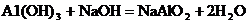 ;氢氧化镁不与氢氧化钠溶液反应。
;氢氧化镁不与氢氧化钠溶液反应。
【提出猜想】利用镁铝与酸、铝与碱、氢氧化铝与碱反应的化学性质来测定合金中镁的质量分数。
【设计方案】研究小组设计了不同的实验方案。
方案l:镁铝合金与过量盐酸反应测定生成气体在标准状况下的体积为V
方案2:镁铝合金与过量NaOH溶液充分反应后,过滤、洗涤、干燥、称量剩余固体的质量为w
方案3:镁铝合金与过量盐酸溶液反应后再与过量NaOH溶液反应,过滤、洗涤、干燥、称量沉淀的质量为w
【问题讨论】请你参与研究小组的研究过程,并回答有关问题:
23.(10分)含镁3%~5%的镁铝合金是轮船制造、化工生产、机械制造等行业的重要原材料。现有一块质量为w g的镁铝合金,某研究性学习小组欲测定其中镁的质量分数。
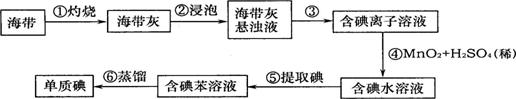
请你填写下列空白:
(1)步骤①灼烧海带时,除需要坩埚、泥三角、三角架外,还需要用到的一种仪器是
(填写序号)。
A.烧杯 B.酒精灯 C.研钵 D.干燥器
(2)步骤②浸泡中,使用了玻璃棒,其作用是 。
(3)步骤③的实验操作名称是 ,该操作中除用到铁架台、烧杯、滤纸外,还用到的仪器是 、 。
(4)实验中用到托盘天平,在使用时,先 ,然后把称量物放在 盘,要用 夹取砝码放在另一盘中。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com