
16.0
9.0
7.0
2.0
加入WgFe2O3
0.8
0.2
30%H2O2溶液
15% H2O2溶液
5% H2O2溶液
加入WgMnO2
30.(7分)甲同学从课外资料得知,不少金属氧化物可做H2O2溶液分解的催化剂,那么,Fe2O3能否作为H2O2分解的催化剂呢?请你一起参与探究,并填写下列空白。
【猜想与假设】Fe2O3能作为H2O2分解的催化剂。
【实验验证】甲同学依次设计了三个实验:
实验一:取一定量的H2O2溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,没有复燃。说明H2O2溶液常温下缓慢分解。
实验二:在实验一的试管中加入WgFe2O3粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃。说明 。
实验三:待反应结束后,将试管里的不溶物滤出,并洗涤干燥、称量,固体质量仍为Wg。说明 。进行过滤操作时,要用到的玻璃仪器有玻璃棒和 、 。为加快过密基速度,甲同学不断搅拌滤液,这样做是否正确,这什么? 。
【实验结论】甲同学认为,Fe2O3粉末可以作为H2O2分解的催化剂。
【反思与评价】乙同学认为要证明甲同学的结论正确,仅做这三个实验还不充分,需要再补充一个探究实验。探究 。
【拓展】下表是丙同学探究影响H2O2分解因素时所记录的部分数据,通过对数据分析,你能得出什么结论?
用足量等体积H2O2溶液制取相同体积O2所需的时间:
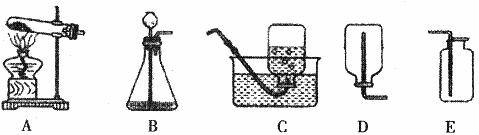
(1)用过氧化氢溶液和二氧化锰制取氧气,该反应的文字表达式 ,应选用的发生装置为 (填字母)。
(2)检验B装置气密性的方法为 。
(3)某同学观察到锥形瓶内有大量气泡时,开始用E装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中和瓶底,都末见木条复燃。其原因是 。
(4)小强想用加热高锰酸钾固体的方法制取并收集纯净的氧气,他应选择的装置为 (填字母)。当氧气收集满并取出集气瓶后,停止该实验的正确操作步骤是先 后 。他这样做的目的是 。
29.(9分)下图是实验室制取气体的部分装置,据图回答有关问题:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com