
2.从
1.探究物质的变化是学习化学的重要内容。下列变化中属于化学变化的是 ( )
A.酒精挥发 B.瓷碗破碎 C.食物腐败 D.石蜡熔化
首先取10 mL该白醋样品,稀释至 100 mL;然后,取稀释后的溶液20 mL用溶质质量分数为0.4%的NaOH溶液中和,当消耗NaOH溶液
应)。
计算:(1)20mL稀释后的溶液中醋酸的质量;
(2)该市售白醋样品中的总酸含量,并说明是否符合国家标准。
29.(7分)国家规定,酿造食醋总酸含量不得低于3.
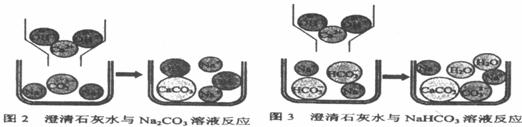
(2)乙同学的两个实验中,大家对CaCl2与Na2CO3溶液的反应比较熟悉,该反应的化学方程式为 ;而对CaCl2与NaHCO3溶液混合产生的现象难以理解,同学们又进一步查阅了资料,了解到CaCl2与NaHCO3溶液可发生如下反应:
CaCl2+2NaHCO3=CaCO3↓+2NaCl+CO2↑+H2O,因而同学们知道了乙同学是通过观察到
现象来鉴别Na2CO3和NaHCO3溶液的。
至于CaCl2与NaHCO3溶液为什么能发生上述反应,老师指出其反应原理较复杂,有待于今后学习中进一步探究。
(3)丙同学在加热Na2CO3固体时,开始产生少量气泡的原因是 ;根据你分析:Na2CO3受热 分解(填“易”或“不易”)。在加热NaHCO3固体时,丙同学观察到的实验现象是
(任写一种)。
【拓展应用】(1)固体Na2CO3中混有少量NaHCO3,可通过 方法除去。
(2)要除去Na2CO3溶液中混有的少量NaHCO3,可加入适量的 溶液。
五、(本题包括1小题,共7分)
【问题讨论】(1)小组同学对上述实验展开了讨论,对甲同学的两个实验进行了比较,并从物质在溶液中解离出不同离子的微观角度分析了原因(如图2、图3)。请写出Na2CO3与澄清石灰水发生反应的化学方程式 ;写出NaHCO3与澄清石灰水混合时参与反应的离子: 。
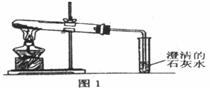
①加热Na2CO3时,开始即见小试管中有少量气泡产生,继续加热,气泡逐渐减少,未见澄清石灰水变浑浊,
②加热NaHCO3时,丙同学观察到实验现象与①不同,证实了自己的猜想是合理的。
28.(13分)某学习小组的同学在学习了Na2CO3、NaHCO3的性质后,了解到它们都能与盐酸反应产生CO2气体,那么如何鉴别Na2CO3和NaHCO3呢?带着这样的疑问,他们进行了下列探究:
【查阅资料】(1)Ca(HCO3)2可溶于水;
(2)NaHCO3固体受热分解生成碳酸钠、二氧化碳和水。
【猜想】(1)甲同学认为可用澄清石灰水鉴别Na2CO3和NaHCO3溶液。
(2)乙同学认为可用CaCl2溶液鉴别Na2CO3和NaHCO3溶液。
甲、乙两同学的猜想是依据澄清石灰水、CaCl2溶液分别与Na2CO3溶液反应均有沉淀产生;又知道Ca(HCO3)2可溶于水,因此猜测澄清石灰水、CaCl2溶液分别与NaHCO3溶液混合不会产生沉淀,从而鉴别出两种溶液。
(3)丙同学认为固体Na2CO3、NaHCO3可用加热的方法鉴别。
【实验探究】(1)甲同学在两支分别盛有少量Na2CO3、NaHCO3溶液的试管中,各加入澄清石灰水,观察到两支试管中的现象相同,均产生了白色沉淀,实验结果与猜想不一致,即不能用澄清石灰水鉴别Na2CO3和NaHCO3溶液。
(2)乙同学将CaCl2溶液加入到分别盛有少量Na2CO3、NaHCO3溶液的试管中,发现两支试管中也都产生了白色沉淀,实验结果出乎意料,但根据观察到的其他实验现象,他认为仍可用CaCl2溶液鉴别Na2CO3和NaHCO3溶液。
(3)丙同学分别取了一定量的Na2CO3、NaHCO3固体于大试管中加热(如图1):
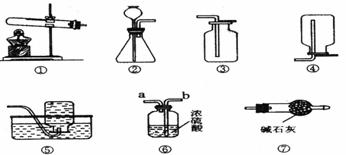
(1)将装置①中的固体加热时应先 ;若用装置⑥净化气体,则气体应从 端通入(填“a”或“b”)。
(2)实验室用过氧化氢溶液和二氧化锰制氧气,应选用的发生装置为 、收集装置为
(填装置的编号),过氧化氢溶液应从 中加入(填仪器名称),其中二氧化锰起 作用。
(3)实验室常用加热氯化铵与氢氧化钙固体混合物的方法制取氨气。通常情况下,氨气的密度比空气小且极易溶于水。若要制得干燥的氨气,则装置的连接顺序为 (填装置的编号)
27.(7分)以下是我们熟悉的实验室制取气体的发生装置、收集装置以及净化装置(装置⑦中碱石灰为固体氢氧化钠和氧化钙的混合物)。请根据装置图回答下列问题:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com