
5.下列物质不属于合金的是
A.不锈钢 B.青铜 C.磁铁矿石 D.生铁
4.下列物质中不属于碱的是
A.纯碱 B.消石灰 C.火碱 D.氢氧化铜
3.下列说法中正确的是
A.浓溶液一定是饱和溶液
B.稀溶液一定是不饱和溶液
C.在一定温度下,析出晶体后的溶液一定是饱和溶液
D.饱和溶液的溶质质量分数一定比不饱和溶液的大
2.关于多金属结核的叙述,正确的是
A.多金属结核是锰的合金
B.多金属结核也称锰结核
C.锰结核中只有一种金属
D.全世界多金属结核含量微乎其微
1.医生建议患甲状腺肿大的病人多食海带等海产品这是因为海带中含有丰富的
A.氟元素 B.碘元素 C.锌元素 D.钙元素
28. 。请计算:
。请计算:
(1)参加反应的碳酸钾的质量。
(2)过滤后所得溶液的溶质质量分数。
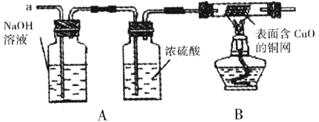
如果放出的是氧气和氢气,你认为方案中的安全隐患是____________________。丙同学认为,为确保安全,实验前应先收集一试管气体,用拇指___________。若不发出__________,方可采用上面的装置进行实验。
实验探究:经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会点燃B处酒精灯,一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色,停止通气,再次称量装置A,发现质量无增减。结论:产生的气体是__________。
思维拓展:
(1)由上述实验可以推出,硫酸铜溶液中可能含有__________物质。
(2)不通过称量,如何判断SO2与氢氧化钠溶液发生了反应呢?有一同学设计了如下图所示装置进行实验,发现试管内液面上升,就得出SO2与氢氧化钠溶液反应的结论。其他同学认为该方案不严谨,理由是______________________________。要得到科学严谨的结论,仍利用该装置,需要补做的实验是___________________。
27.某化学实验小组的同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡冒出。这一现象激起同学们探究的欲望,生成的气体是什么气体?
提出猜想:从物质组成元素的角度,生成的气体可能是SO2、O2、H2。
查阅资料:SO2易溶于水,能与氢氧化钠溶液反应,生成Na2SO3。
方案设计:依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是氧气,则检验方法是____________________________________。
(2)乙同学认为是SO2,则只需将放出的气体通入盛有氢氧化钠溶液的洗气瓶中,称量通入气体前后洗气瓶的质量。写出SO2与氢氧化钠反应的化学方程式________ ________________________________________。
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
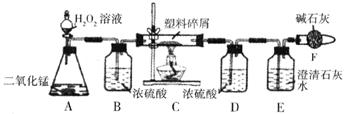
(1)仪器A中所发生反应的化学方程式____________________________________。
(2)仪器B的作用是____________________________________________________。
(3)仪器E中的现象是__________________________________________________。
(4)若仪器C的玻璃管中放入的塑料试样质量为Wg,塑料试样充分燃烧后,若仪器D增重a g,Wg该塑料试样中含氢元素的质量为________g(结果可用分数表示)。
(5)若装置中没有连接仪器B,将使该塑料试样中含氢元素的质量测算结果________(填偏小、偏大或无影响)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com