
1.日常生活中见到下列现象,其中发生了化学变化的是
A.冬天的早晨,玻璃窗上出现美丽的冰花 B.自行车轮胎在烈日下爆裂
C.牛奶放置时间过长变质 D.玻璃杯被打碎
(2)计算Na2CO3溶液中溶质的质量分数。(计算结果精确到0.1%)
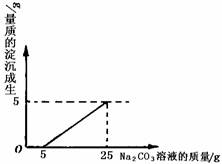
(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,说明滤液中的溶质除含有CaCl2外,还含有______________________;
35.(3分)刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数。他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如下图所示。
(Na2CO3+CaCl2= CaCO3↓+2NaCl)
(2)若加入含氧化钙5.6t的生石灰,理论上最多可吸收二氧化硫多少吨?
(1)请完成该反应的化学方程式:2CaO+2SO2+
 2CaSO4
2CaSO4
34.(3分)向原煤中加入适量生石灰可有效地减少二氧化硫的排放,削弱二氧化硫对空气的污染。
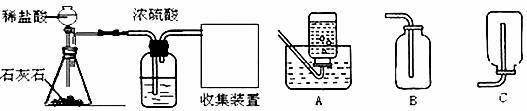
(1)实验室制取CO2的化学方程式为 ,浓硫酸的作用是 ,收集装置为 (填字母)。
(2)化学课上,李芹同学将燃烧的钠迅速伸入盛有CO2的集气瓶中,钠在集气瓶中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
[提出问题]黑色颗粒和白色物质可能是什么呢?
[进行猜想]你认为黑色颗粒是_____________,小明认为白色物质是氧化钠,小艺认为是碳酸钠,小亮认为是氧化钠和碳酸钠的混合物,小华认为是氢氧化钠。
李芹同学认为小华的猜想是错误的,其理由是__________________。
[查阅资料]CaCl2+Na2CO3=CaCO3↓+2NaCl ,氧化钠为白色粉末,溶于水生成氢氧化钠。
[实验探究]李芹同学对白色物质进行实验探究。
实验方案1:取该样品少量于试管里,加适量水,振荡,样品全部溶于水。向其中加入无色酚酞试液,观察到溶液变成红色。结论:白色物质为氧化钠。
实验方案2:取该样品少量于试管里,加适量水,振荡,样品全部溶于水。向其中加入过量的CaCl2溶液,出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现。结论:白色物质为____________________。
[反思评价]小娟同学认为实验方案1得出的结论不正确,其理由是_____________。
[得出结论]钠在二氧化碳中燃烧的化学方程式为_____________。
33.(8分)为探究CO2的化学性质,需要制取并收集干燥的CO2,以下是老师提供的一些实验装置。

【实验探究】请你帮助他们写成实验报告。
实验步骤
实验现象
实验结论及化学方程式
点燃酒精灯加热,随即打开弹簧夹,通入干燥的空气。
观察装置B、装置C中的现象
装置B中的现象是:
装置C中的现象是:
聚乙烯塑料在空气中燃烧,生成碳的氧化物中,既有CO2,也有CO。
装置C中反应的化学方程式为:
【讨论】
(1)根据实验结论,从环保角度考虑,实验中应对尾气进行处理。处理方法是 。
(2)聚乙烯塑料在空气中燃烧,生成物中除了CO2、CO外,还应有的物质是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com