
19.(8分)过氧化氢是一种化学性质不稳定的物质。实验室里现有一瓶久置的过氧化氢消毒液,为测定其溶质的质量分数,某化学活动小组的同学做了如下实验:称取
18.(5分)某化学兴趣小组的同学在实验室里对二氧化硫气体的性质进行探究,他们向盛有二氧化硫气体的集气瓶中倒入一定量的水,振荡后用胶头滴管吸取该液体滴在蓝色石蕊试纸上,发现蓝色石蕊试纸变成红色。姜华同学根据已有的知识,断定是二氧化硫气体与水反应生成的酸使石蕊试纸变红。
从科学探究的角度看,你认为姜华的判断是否严密?____________________。你的理由是__________________________________________________。
请针对你的理由设计实验方案进行验证。(指示剂限用蓝色石蕊试纸)
(Ⅱ)
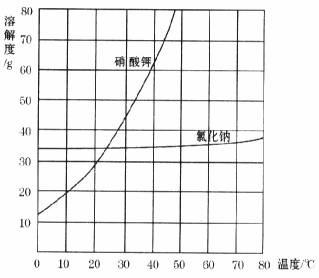
过去民间燃放的鞭炮都是黑火药制成的。在制备黑火药时,硝酸钾是一种关键物质。硝酸钾俗称火硝,主要存在于硝土中(硝土的成分有硝酸钾、硝酸钙、氯化钠及一些难溶性的固体物质等)。
传统的提取粗硝酸钾的过程按以下步骤进行:
(1)溶解。将硝土与豆秆灰(豆秆灰的成分中含碳酸钾及一些难溶性的固体)按一定的质量比混合,常温下加入足量的水并进行充分搅拌。其中发生化学变化的相关反应的化学方程式为_____________________________。
(2)接下来要进行的操作是__________,便可得到澄清的液体A。为了最大限度地得到硝酸钾,通常要加入稍过量的豆秆灰,如何通过实验证明加入的豆秆灰已过量?
______________________________________________________________________。
(3)蒸发浓缩。将第(2)步操作中得到的液体A进行加热蒸发浓缩,析出晶体X,你认为晶体X的主要成分是什么? __________,理由是__________________。若在实验室进行本操作,需要的主要仪器有____________________。
(4)过滤。将第(3)步操作中得到的混合物趁热过滤滤出晶体X,得到滤液B。
(5)最后对滤液B进行____________________,然后过滤,便可分离出晶体Y,晶体Y的主要成分是______________________________。
16.(8分)随着时代的发展,金属材料的应用越来越广泛。下表提供了几种常见金属的有关信息,根据表中提供的信息回答下列问题:(导电性以银的导电性为100作标准)
金属
颜色
熔点/℃
导电性
化学性质
Al
银白色
660
61
常温下易与氧气反应,表面形成致密的氧化膜
Fe
银白色
1 535
17
在潮湿的空气中容易生锈
Cu
紫红色
1 083
99
在高温时能与氧气反应
(1)铜钱在历史上曾是一种广泛流通的货币,你认为用铜而不用铁来铸造货币的主要原因有哪些?___________________________________________________。
(2)铝比铁更易与氧气或其他物质发生化学反应,但为什么铝制品不易被腐蚀?
_______________________________________________________________
(3)铁在自然界中主要以化合物的形式存在,请写出工业上以赤铁矿为原料炼铁的化学反应原理(用化学方程式表示)________________________________________________。
(4)生产中通常将铬、镍等金属熔合在铁中制成不锈钢改变其组成和结构,达到防止铁制品生锈的目的,这一事例说明了一个重要的化学观念或化学道理,即物质的__________决定物质的____________。
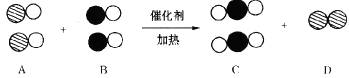
(1)从宏观上看A和B两种物质在组成上的相同点是_________________。
(2)从微观上看C和D两种物质在构成上的不同点是_________________。
(3)分别从宏观和微观两个角度描述该化学变化___________;__________。用化学反应方程式表示为_________________;化学变化过程中消耗的A物质和生成的C物质的质量比为_________________。
(4)从微观的角度描述你获得的关于化学变化的有关信息(答出一条即可)
____________________________________________________________________。
15.(10分)在宏观――微观――符号之间建立联系,是化学学科特有的思维方式。汽车尾气是造成大气污染的主要原因之一。在汽车排气管上安装“催化转换器”便可以将汽车的尾气转换成无毒的气体。如果用“●”表示碳原子,用“○”表示氧原子,用“ ”表示氮原子,下图为气体转换的微观过程,请你根据图示回答下列问题:
”表示氮原子,下图为气体转换的微观过程,请你根据图示回答下列问题:
14.(4分)分类法是科学研究的一种重要方法,分类标准有多种,化学上可从不同的角度对物质进行分类。请按要求完成下列问题:
(1)下列两组物质中均有一种物质所属类别与其他两种不同,请选出该物质,用化学式表示,并说明选择的理由。
①纯碱、熟石灰、硫酸铜:
选出的物质是__________ ,理由是____________________。
②铜、汞、金:
选出的物质是__________,理由是____________________。
(2)仿照以上形式,以构成物质粒子的种类为分类标准,从你所了解的物质中选择适当物质填到下列横线上:__________、__________、__________;其中不同类的物质是(用化学式表示)__________,理由是______________________________。
A.4 B.
(5)三聚氰胺在类别上属于__________。
A.混合物 B.有机物 C.无机物 D.碱
(6)验证三聚氰胺水溶液显碱性可以用__________。
A.紫色石蕊试液 B.无色酚酞试液
C.蓝色石蕊试纸 D.pH试纸
⑤
熔点
⑥
酸碱性
水溶液呈弱碱性
⑦
稳定性
一般情况下较稳定,高温下能分解放出有毒的氰化物
⑧
用途
用作生产三聚氰胺甲醛树脂的原料,还可以作阻燃剂等
试回答下列问题:
(1)三聚氰胺的相对分子质量为__________,每个分子中原子的总数为__________,碳、氮元素的质量比为__________。
(2)在上表给出的信息中,属于三聚氰胺化学性质的有____________________(填编号)。
(3)
(4)测定三聚氰胺水溶液的pH约为__________(填序号,下同)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com