
称取7.
答:样品中硫酸铵的庸量分数为94.3%
小昊通过实验测得有关数据,然后进行计算,过程如下:
x=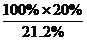 =94.3%
=94.3%
100%:21.2%=x:20.0%
=21.2%
设样品中硫酸铵的纯度为x
=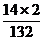 ×100%
×100%
 ×100%
×100%
含氮量:20.0%
生产日期:
小玉根据标签所示的含氮量直接进行理论计算,过程如下:
解:硫酸铵中氮元素的质量分数:
17.(5分)肥田粉是常用的氮肥,图为某品牌肥田粉的部分标签,为了计算该品牌肥田粉的纯度(硫酸铵的质量分数),小玉和小昊采用了两种不同的方法。
×××牌肥四份
有效成分:硫酸铵(NH4)2SO4
16.(6分)通过学习氧气的性质,知道镁在氧气中燃烧会生成白色固体物质。但某学习小组的同学发现在空气中点燃镁条时,生成的白色固体物质中夹杂着少量的淡黄色固体。为了探究其原因,他们做了以下工作:
[提出问题]淡黄色固体物质的成分是什么?
[查阅资料]通过查阅资料,记录了下列几种物质的颜色:
物质
MgO
MgCl2
Mg3N2
Mg(NO3)2
MgCO3
Mg(OH)2
颜色
白色
白色
淡黄色
白色
白色
白色
某同学推断产物中一定不存在氯化镁,你认为他的理由是_____________;
[提出猜想]分析以上资料,同学们认为淡黄色的固体可能是镁与空气中的_________(填写化学式)反应生成的;
[实验探究]如果让你设计实验验证上述猜想,你的方案是__________________
[实验结论]根据实验结果,写出镁条在空气中燃烧时发生反应的化学方程式: _____________、____________
[反思与评价]通过上述探究,你对燃烧的新认识是____________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com