
2.
A.①②④⑤ B.①②③⑤ C.①②③④ D.①②④⑤
1.日常生活中发生的下列变化,属于化学变化的是
A.纸张粉碎 B.蜡烛燃烧 C.冰雪融化 D.酒精挥发
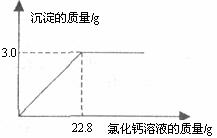
求:(1)该纯碱样品中碳酸钠的质量分数。
(2)所加入氯化钙溶液的溶质质量分数。
30.(8分)用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠。为测定某纯碱样品中碳酸钠的含量,小玉称取该纯碱样品
(2)要配制
(1)
29.(4分)为了防止流感的传播,某医院每天需要喷洒大量的过氧乙酸液消毒。
28.(8分)小明在做某次实验时,发现一瓶瓶口已敞开不知多久的氢氧化钠溶液(下称试液)。联想到药品保存注意事项,小明利用提供的试剂(CaCl2溶液、盐酸、CaCO3固体、酚酞)对试液是否变质展开了探究。
他首先猜想的是:试液没有变质,溶液的溶质还是NaOH,根据实验方案进行的实验:
①取少量试液加入试管,滴入酚酞,观察到试液变红。由此得出结论是原试液没有变质,还是NaOH。
②小明反思实验验证,觉得不够完善,理由是_________________________________。
③完善实验方案后他从提供的试剂中选取一种试剂进行实验。发现原试液确已变质。请你写出他这次实验的操作:____________________,现象是:____________________。小明是个爱思考的学生,他又有一个新的疑问:试液中真的没有NaOH了吗?他又做了进一步探究:
④猜想_______________________________________________________。
⑤实验验证:实验操作_________________________________;实验现象____________ ______________________,实验结论_________________________________。
⑥通过探究,小明明白了:氢氧化钠溶液暴露在空气中会变质,故应___________保存。
六、计算题(本题包括2个小题,共12分)
27.(8分)某化学兴趣活动小组的同学想探究某温度下氯化钠溶液的酸碱度,过程如下:
【猜想与假设】溶液的pH可能为①pH<7;②___________;③___________。
【设计与实验】要测定该溶液的酸碱度,除有正确的操作步骤外,其中不能采用下列物质中的___________(填序号)来进行实验。
①pH试纸 ②紫色石蕊试液 ③酚酞试液
组内同学进行了如下实验:
甲同学:取pH试纸放在玻璃片上,用玻璃棒蘸取氯化钠溶液沾在pH试纸上,把试纸显示的颜色与标准比色卡片比较,测得pH=7
乙同学:pH试纸放在玻璃片上,先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取氯化钠溶液沾在pH试纸上,把试纸显示的颜色与标准比色卡片比较,测得pH=7
丙同学:将pH试纸直接浸入氯化钠溶液中,把试纸显示的颜色与标准比色卡片比较,测得pH=7
【评价与反思】三位同学中操作正确的是___________,指出其他同学的操作错误:__________________________________________。
【结论与分析】丙同学得出“凡是盐溶液的pH都等于
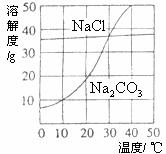
(1)当温度为
(2)当温度___________时,氯化钠的溶解度大于碳酸钠的溶解度;
(3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”。请你解释原因:“夏天晒盐” _______________________;(2分)“冬天捞碱” ____________________。(2分)
五、实验探究题(本题包括2个小题,每空1分,共16分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com