
12、__________________;
9、__________________;10、__________________;11、__________________;
40?X*20% =36.5?
X=
答:烧碱溶液的质量为
X*20%
40 36.5
38.(4分) (1) 15:3:20 ------- 2分 (2) 152 --------2分
39 (6分)(1)10% 2分
(2)解:设烧碱溶液的质量为X
NaOH + HCl ====== NaCl + H2O ------1分
37. (6分)(1)不同意,因为常温下氢氧化钙微溶于水,该白色粉末也可能是没有变质的氢氧化钙。 1分
(2)小明:该白色粉末有氢氧化钙和碳酸钙组成的。 1分
小方:白色粉末是氢氧化钙。 1分
(3)
实验步骤
实验现象
实验结论
取样,加适量水,搅拌,过滤
①取少量滤液于试管中,滴入酚酞试液
②取少量滤渣与试管中,加入盐酸
①滤液变红
② 有气泡产生
该瓶氢氧化钙已经部分变质了。(或该药品是由氢氧化钙和碳酸钙组成的。)
(小方的方案可参考上述步骤)
五、计算题(共8分)
【拓展交流】N2(或稀有气体)(1分)
36 .(5分)
(2)塑料瓶被压瘪;注射器中剩余的10mL NaOH溶液立即“自动”进入塑料瓶中;
瓶中的CO2与NaOH溶液反应不断被消耗,气体压强减小,外界大气压将塑料瓶压瘪,同时将剩余的NaOH溶液压入瓶中。 2分
(3)由于反应容器密闭,生成物全部留在瓶中,也没有空气进入,因而反应前后质量相等(即质量守恒) 1分
(4) ①若采用有气体参加或生成的反应来验证质量守恒定律,应让化学反应在密闭容器中进行;1分
②向反应后的溶液中滴加稀盐酸(或稀硫酸)看到有气泡产生(或向反应后的溶液中滴加BaCl2溶液看到有白色沉淀产生。)(其他合理答案可给分)1分
35.(5分)【猜想与假设】:(3) Cu,CO2和CO(1分)
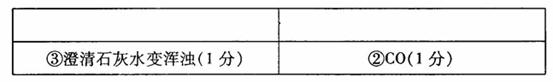
【设计方案】(1)产生的气体通入澄清石灰水,观察是否变浑浊(1分)
【实验与结论】
34 .(5分)(1) 2KMnO4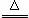 K2MnO4+MnO2+O2↑ (2)
D、E
K2MnO4+MnO2+O2↑ (2)
D、E
(3) 可以控制反应数率 (4)过滤;漏斗
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com