
| 不定项 |
| 下列关于胶体的叙述正确的是 |
A.布朗运动是胶体微粒特有的运动方式,可以据此把胶体、溶液和悬浊液区分开来 B.胶体和溶液的本质区别是胶体能发生丁达尔现象 C.用渗析的方法净化胶体时,使用半透膜只能让小分子和离子通过 D.胶体带电,故在电场作用下会产生电泳现象 |
科目:高中化学 来源: 题型:
 右图是一种航天器能量储存系统原理示意图。
右图是一种航天器能量储存系统原理示意图。
下列说法正确的是
A.该系统中只存在3种形式的能量转化
B.装置Y中负极的电极反应式为:
![]()
C.装置X能实现燃料电池的燃料和氧化剂再生
D.装置X、Y形成的子系统能实现物质的零排放,
并能实现化学能与电能间的完全转化
科目:高中化学 来源: 题型:
在《圣经·出埃及记》中就已经提到了单质X,为了研究X及其化合物的性质,进行了如下实验:将准确称量的等质量的物质A和B置于充满氩气的容器中充分混合。将容器密闭(p=1.01×105Pa,T=291K)并加热。反应停止后,容器内的压强等于2.66×105Pa(T=300K),而反应的唯一固体产物是一种单质X。在空气中加热氧化物A导致如下的质量损失(相对于起始质量):
| 温度,K | 566 | 624 | 647 | 878 |
| 质量损失,% | 2.789 | 3.905 | 4.463 | 6.695 |
| 生成的物质 | C | D | F | G |
下图还表示了各物质之间的相互转化关系(图中省略了部分物质),B呈黑色,Z呈黄色。

(1)试确定A、F、L、Q、Z的化学式
(2)写出下列化学方程式①A +B;②G + KCN
(3)若容器的容积等于1.00L,试确定所称取的物质A的质量。
科目:高中化学 来源: 题型:
正极材料为![]() 的锂离子电池被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
的锂离子电池被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
(1)橄榄石型![]() 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过![]() 、
、![]() 与
与![]() 溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而值得。
溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而值得。
①共沉淀反应投料时,不将![]() 和
和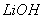 溶液直接混合的原因是 _。
溶液直接混合的原因是 _。
②共沉淀反应的化学方程式为 _。
③高温成型前,常向![]() 中加入少量活性炭黑,其作用除了可以改善成型后的
中加入少量活性炭黑,其作用除了可以改善成型后的![]() 的导电性能外,还能 _。
的导电性能外,还能 _。
(2)废旧锂离子电池的之极材料试样(主要含有![]() 及少量AI、Fe等)可通过下列实验方法回收钴、锂。
及少量AI、Fe等)可通过下列实验方法回收钴、锂。
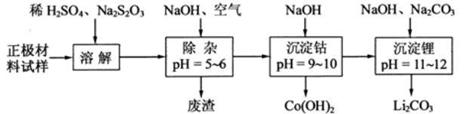
 在上述溶解过程中,
在上述溶解过程中,![]() ,
,![]() 在溶解过程中反应的化学方程式为 _。
在溶解过程中反应的化学方程式为 _。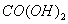 在空气中加热时,固体残留率随温度的变化如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余故土成分为 _。(填化学式);在350~400℃范围内,剩余故土成分为 _。(填化学式)。
在空气中加热时,固体残留率随温度的变化如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余故土成分为 _。(填化学式);在350~400℃范围内,剩余故土成分为 _。(填化学式)。
科目:高中化学 来源: 题型:
对乙酰氨基酚,俗称扑热息痛(Paracetamol),具有很强的解热镇痛作用,工业上通过下列方法合成(B1和B2、C1和C2分别互为同分异构体,无机产物略去):请按要求填空:
(1)上述①~⑤的反应中,属于取代的有__________________(填数字序号)。
(2)C2分子内通过氢键又形成了一个六元环,C1只能通过分子间氢键缔合,工业上用水蒸气蒸馏法将C1和C2分离,则首先被蒸出的成分是______(填“C1”或“C2”)。
(3)工业上设计反应①、②、③得到C1、C2,而不是只通过苯酚与硝酸反应直接得到C1、C2,其目的是______________________________________________________。
(4)扑热息痛有很多同分异构体,符合下列要求的同分异构体有5种:(I)是对位二取代苯;(Ⅱ)苯环上两个取代基一个含氮不含碳、另一个含碳不含氮;(Ⅲ)两个氧原子与同一原子相连;其中2种结构是![]() 和
和![]() ,写出另外3种同分异构体的结构简式
,写出另外3种同分异构体的结构简式
_______________________________________________________________________。
科目:高中化学 来源: 题型:
高炉炼铁过程中发生的主要反应为
![]()
已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的平衡常数表达式K=_____________,△H________0(填“>”.“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe.Fe2O3.CO.CO2各1.0mol,反应经过l0 min后达到平衡。求该时间范围内反应的平均反应速率υ(C02)=_____________.CO的平衡转化率=_____________:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是_____________。
A.减少Fe的量 B.增加Fe203的量 C.移出部分C02
D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂
科目:高中化学 来源: 题型:
生活中常会碰到的某些化学问题,例如:①“白雪牌”漂粉精可令所有有色物质黯然失“色”,没有最白,只有更白;②霸王洗发液不含任何化学物质;③人喝了啤酒会打嗝,是因为啤酒中的碳酸盐与胃酸反应生成了二氧化碳;④53度白酒是指该白酒的着火点是53℃;
⑤三鹿奶粉中的三聚氰胺是一种高分子化合物;⑥太太口服液含丰富的氮、磷、锌等微量元素 有关上述说法,你的看法是 ( )
A.全部正确 B.只有①⑤正确
C.只有③⑤⑥正确 D.以上说法都是错误的
科目:高中化学 来源: 题型:阅读理解
现有X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素。有关信息如下表:
|
| 原子或分子相关信息 | 单质及其化合物相关信息 |
| X | ZX4分子空间结构为正四面体 | X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y | Y原子的最外层电子数等于电 | Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料(人造刚玉) |
| Z | Z原子的最外层电子数是次外层电子数的 | Z是无机非金属材料的主角,其单质为原子晶体,是一种优良的半导体材料 |
| W | W原子的最外层电予数小于4 | W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(1)W位于周期表第四周期第 族,W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为 。
(2)Z最简单的氧化物分子是 分了(填“极性”或“非极性”):工业上用Z的氧化物制备其单质的化学反应方程式为 。
锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它最常用来制造晶体篱,最新研究表明:有机锗具有明显的抗肿瘤活性,锗元素的最高价氧化物的化学式为 。
(3)实验室制取X单质的离子方程式为 ;X的气态氧化物的水溶液与Y的氧化物反应的离子方程式为 。
(4)在50mL lmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能为 mL或 mL。
科目:高中化学 来源: 题型:
应用纳米新材料能给人民币进行杀菌、消毒。我国纳米专家王雪平发明的“WXP”复合纳米材料”的主要化学成份是氨基二氯代戊二醛含硅衍生物,它能保持长期的杀菌作用。有鉴于此,35位人大代表联名提交了一份议案,要求加快将此新技术应用到人民币制造中去。若戊二醛是直链的,请你5根据所学的知识推断沸点不同的氨基二氯代戊二醛的同分异构体可能有 ( )
A.4种 B.5种 C.6种 D.8种
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com