
| 不定项 |
| 第三周期元素的原子,其最外层p能级上仅有一个未成对电子,它最高价氧化物对应的水化物的酸根离子是 |
A.RO3- B.RO5- C.RO42- D.RO4- |
科目:高中化学 来源: 题型:阅读理解
| 元素编号 | 元素性质或原子结构 |
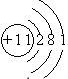
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
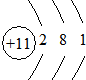
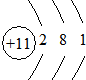
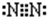
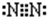
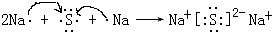
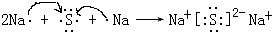
| O2 |
| O2 |
| H2O |
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子气态分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |



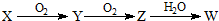
科目:高中化学 来源: 题型:
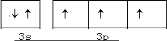

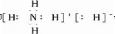
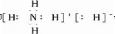
科目:高中化学 来源:2013-2014学年湖北省荆州市高三毕业班质量检查(二)理综化学试卷(解析版) 题型:填空题
已知A、B、C、D、E、F、G为前四周期七种元素且原子序数依次增大,其中A的基态原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,C原子核外成对电子数比未成对电子数多1个,其氢化物常用作致冷剂,D原子未成对电子与周期数相同,在E元素所在周期中的基态该原子的第一电离能最小;F原子价电子nsn-lnpn+l;G单质是硬度最大的金属。
请回答下列问题:
(1)G元素基态原子价电子排布式为??????????????????????? 。
(2)B、C、D三种元素的最简单氢化物的键角由小到大的顺序为____?????? (填元素符号),常温下硬度最大的B单质、E2F、H2D及H2F的沸点由大到小的顺序为____??? (填化学式)
(3)D元素与氟元素相比,电负性:D?????????? 氟元素(填“>”、“=”或“<”),?? 下列表述中能证明这一事实的是????????????? (填选项序号)-
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)离子化合物CA5的晶体中含有多种化学键:但一定不含有的化学键是????????? (填选项序号)。
A.极性键?????? B.非极性键?????? C.配位键?????? D.金属键
(5)B2A4是重要的基本石油化工原料。B2A4分子中B原子轨道的杂化类型为____???? ;1molB2A4分子中含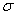 键???????? mol。
键???????? mol。
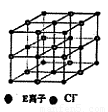
(6)如图是E的氯化物的晶胞示意图,最近两个E离子之间距离为a cm,则该晶体密度为?????????? (已知阿伏加德罗常数为NA).
科目:高中化学 来源:不详 题型:填空题
 键 mol。
键 mol。
科目:高中化学 来源:崇明县一模 题型:问答题
| 键能(kJ/mol) | 键能(kJ/mol) | 键能(kJ/mol) | |||
| H-H | 436 | C-Cl | 243 | H-Cl | 432 |
| Cl-Cl | 330 | C-I | 218 | C-F | 427 |
| C-O | 347 | H-O | 464 | H-F | 565 |
| 选项 | 现象:沸点H2O>H2S | 原理:键能H-O>H-S | 原理对现象的解释 |
| A | 正确 | 正确 | 可以 |
| B | 错误 | 正确 | |
| C | 正确 | 错误 | |
| D | 正确 | 正确 | 不可以 |
科目:高中化学 来源:2011年上海市崇明县高考化学一模试卷(解析版) 题型:解答题
| 键能(kJ/mol) | 键能(kJ/mol) | 键能(kJ/mol) | |||
| H-H | 436 | C-Cl | 243 | H-Cl | 432 |
| Cl-Cl | 330 | C-I | 218 | C-F | 427 |
| C-O | 347 | H-O | 464 | H-F | 565 |
| 选项 | 现象:沸点H2O>H2S | 原理:键能H-O>H-S | 原理对现象的解释 |
| A | 正确 | 正确 | 可以 |
| B | 错误 | 正确 | |
| C | 正确 | 错误 | |
| D | 正确 | 正确 | 不可以 |
科目:高中化学 来源: 题型:
| 键能(kJ/mol) | 键能(kJ/mol) | 键能(kJ/mol) | |||
| H-H | 436 | C-Cl | 243 | H-Cl | 432 |
| Cl-Cl | 330 | C-I | 218 | C-F | 427 |
| C-O | 347 | H-O | 464 | H-F | 565 |
| 选项 | 现象:沸点H2O>H2S | 原理:键能H-O>H-S | 原理对现象的解释 |
| A | 正确 | 正确 | 可以 |
| B | 错误 | 正确 | |
| C | 正确 | 错误 | |
| D | 正确 | 正确 | 不可以 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com