
科目:高中化学 来源:不详 题型:单选题
| A.因为p轨道是“8”字形的,所以p电子走“8”字形 |
| B.第三电子层,有3s、3p、3d三个轨道 |
| C.原子轨道与电子云都是用来形象描述电子运动状态 |
| D.氢原子中只有一个电子,故氢原子只有一个轨道 |
科目:高中化学 来源:2012-2013学年江苏省启东中学高二下学期期中考试化学试卷(带解析) 题型:单选题
下列说法正确的是( )
| A.因为p轨道是“8”字形的,所以p电子走“8”字形 |
| B.第三电子层,有3s、3p、3d三个轨道(答案只选D,可B应该是正确的) |
| C.铝元素原子核外共有5种不同运动状态的电子 |
| D.电离能最小的电子能量最高 |
科目:高中化学 来源:2014届江苏省高二下学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.因为p轨道是“8”字形的,所以p电子走“8”字形
B.第三电子层,有3s、3p、3d三个轨道(答案只选D,可B应该是正确的)
C.铝元素原子核外共有5种不同运动状态的电子
D.电离能最小的电子能量最高
科目:高中化学 来源:不详 题型:单选题
| A.因为p轨道是“8”字形的,所以p电子走“8”字形 |
| B.第三电子层,有3s、3p、3d三个轨道(答案只选D,可B应该是正确的) |
| C.铝元素原子核外共有5种不同运动状态的电子 |
| D.电离能最小的电子能量最高 |
科目:高中化学 来源: 题型:
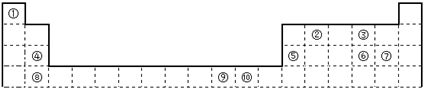
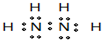
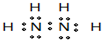
| 电子能I(Ev) | A | B | C | D | E | F |
| I1 | 11.3 | 14.5 | 13.6 | 5.2 | 7.6 | 6.0 |
| I2 | 24.4 | 29.6 | 35.1 | 49.3 | 15.0 | 18.8 |
| I3 | 47.9 | 47.4 | 54.9 | 71.6 | 80.1 | 28.4 |
| I4 | 64.5 | 77.5 | 77.4 | 98.9 | 109.2 | 112.0 |
| I5 | 392.1 | 97.9 | 113.9 | 138.3 | 141.3 | 153.7 |
科目:高中化学 来源: 题型:阅读理解

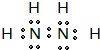
| 电离能I(eV) | A | B | C | D | E | F |
| I1 | 11.3 | 14.5 | 13.6 | 5.2 | 7.6 | 6.0 |
| I2 | 24.4 | 29.6 | 35.1 | 49.3 | 15.0 | 18.8 |
| I3 | 47.9 | 47.4 | 54.9 | 71.6 | 80.1 | 28.4 |
| I4 | 64.5 | 77.5 | 77.4 | 98.9 | 109.2 | 112.0 |
| I5 | 392.1 | 97.9 | 113.9 | 138.3 | 141.3 | 153.7 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com