
科目:高中化学 来源: 题型:
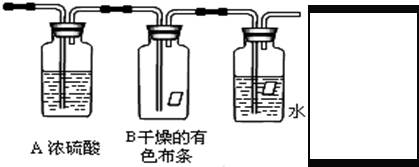
科目:高中化学 来源: 题型:阅读理解

| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 5.8 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 8.8 | 3.2 | 5.2 | 6.7 |
2- 3 |
2- 6 |
科目:高中化学 来源:2012-2013学年江苏省无锡市高三上学期期末考试化学试卷(解析版) 题型:实验题
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某化学兴趣小组将一批废弃的线路板简单处理后,得到主要含Cu、Al及少量Fc、Au、Pt等金属的混合物,设计了如下制备硫酸铜晶体和硫酸铝晶体的路线:
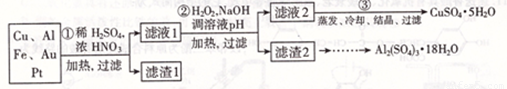
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表
|
沉淀物 |
Fe( OH)2 |
Fe( OH)3 |
Al( OH)3 |
Cu( OH)2 |
|
开始沉淀 |
5.8 |
1.1 |
4.0 |
5.4 |
|
完全沉淀 |
8.8 |
3.2 |
5.2 |
6.7 |
请回答下列问题:
(1)第①步操作前需将金属混合物进行粉碎,其目的是 ;
(2)某学生认为用H2O2代替浓HNO3更好,理由是 ;
请写出Cu溶于H2O2与稀硫酸混合溶液的离子方程式是 。
(3)第②步中应将溶液pH调至 。
(4)由滤渣2制取Al2( SO4)3.18H2O,探究小组设计了两种方案:
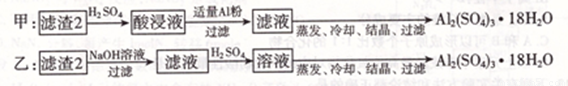
你认为 种方案为最佳方案,理由是 、 。
(5)为了测定硫酸铜晶体的纯度,某同学准确称取4.0g样品溶于水配成l00mL溶液,取l0m溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.l000mol·L-1Na2S2O3标准溶液滴定至终点,共消耗14. 00mL Na2S2O3标准溶液。上述过程中反应的离子方程式如下:
2Cu2+ +4I-=2CuI(白色)↓+I2
2S2O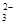 +I2=
2I-+S4O
+I2=
2I-+S4O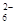
①样品中硫酸铜晶体的质量分数为____ 。
②另一位同学提出通过测定样品中硫酸根离子的量也可求得硫酸铜晶体的纯度,其他同学认为此方案不可行,理由是 。
科目:高中化学 来源: 题型:
(1)下列实验设计或操作均有不妥之处,其中存在安全隐患或可能产生安全事故的是_______。
①直接点燃未检验纯度的CO
②石油分馏实验时,不加沸石直接加热蒸馏
③用混有炭粉的二氧化锰与氯酸钾混合加热制氧气
④在稀释浓硫酸时,将水直接倒入浓硫酸中
⑤制Cl2用1 mol·L-1盐酸与MnO2作用
(2)已知KMnO4(158.0 g·mol-1)可将草酸根离子完全氧化成二氧化碳,因此草酸根离子常被用以测定高锰酸钾溶液的浓度:

![]() +
+![]() +16H+
+16H+![]() 2Mn2++10CO2↑+8H2O,现称取0.670 0 g的草酸钠(134.0 g·mol-1)溶于约30 mL水中,加入10 mL稀硫酸(3 mol·L-1)后趁热以高锰酸钾溶液滴定。试完成下列问题:
2Mn2++10CO2↑+8H2O,现称取0.670 0 g的草酸钠(134.0 g·mol-1)溶于约30 mL水中,加入10 mL稀硫酸(3 mol·L-1)后趁热以高锰酸钾溶液滴定。试完成下列问题:
①滴定时KMnO4溶液应盛放在_________滴定管中,测定后的溶液应保存在_________试剂瓶中(填:“棕色”或“无色”)。
②如何判断恰好完全反应____________________。
③开始时滴定管液面恰好处于“0”刻度处(此滴定管最小刻度为0.1 mL),到滴定终点时,处于图示位置,体积读数为: _________mL;根据以上数据计算出KMnO4溶液物质的量浓度为_________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com