
科目:高中化学 来源: 题型:阅读理解
 铜是人类最早使用的金属,被广泛应用于电气、轻工、机械制造和国防工业等.已知Cu2O与H2SO4能发生反应:Cu2O+H2SO4=Cu+CuSO4+H2O.
铜是人类最早使用的金属,被广泛应用于电气、轻工、机械制造和国防工业等.已知Cu2O与H2SO4能发生反应:Cu2O+H2SO4=Cu+CuSO4+H2O.
| ||
科目:高中化学 来源: 题型:
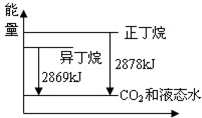 已知在相同条件下1mol正丁烷和1mol异丁烷完全燃烧生成CO2和液态水,放出的热量如图所示,则下列说法正确的是( )
已知在相同条件下1mol正丁烷和1mol异丁烷完全燃烧生成CO2和液态水,放出的热量如图所示,则下列说法正确的是( )| A、1mol正丁烷比1mol异丁烷完全燃烧放出的热量少9 kJ | B、正丁烷分子储存的能量大于异丁烷 | C、异丁烷转化为正丁烷的过程是一个放热过程 | D、异丁烷分子中的碳氢键比正丁烷多 |
科目:高中化学 来源: 题型:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com