
科目:高中化学 来源:2011年上海市黄浦区市南中学高考化学模拟试卷(解析版) 题型:选择题
科目:高中化学 来源:不详 题型:单选题
| A.合成氨工业与接触法制硫酸中的SO2的催化氧化过程中都采用了高压的生产条件 |
| B.结构陶瓷碳化硼(B4C3)常用于制造切削工具,它是一种新型无机非金属材料,属于原子晶体 |
| C.光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅 |
| D.氟利昂和NOx都能破坏臭氧层,从而导致“温室效应” |
科目:高中化学 来源: 题型:
下列有关化工生产的说法正确的是( )
A.合成氨、接触法制硫酸工业中都应用了高温、高压、催化剂为条件
B.三峡大坝使用了大量水泥,水泥属于一种新型无机非金属材料
C.接触法硫酸工业中,炉气进入接触室之前需要净化、干燥,因为炉气中的杂质易与SO2反应
D.工业“三废”的综合利用不仅减少污染,还获得有用的副产品
科目:高中化学 来源: 题型:
(20分)
(I)多项选择题(6分)
下列关于水处理的说法正确的是 。
A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程
B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度
C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术
D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化
E.电渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
(II)(14分)
下列是工业合成氨的简要流程示意图:
请回答下列问题:
(1)H2通常用碳氢化合物与水反应,写出有关的反应方程式 ,从冷凝器回流到压缩机中的X是 。
(2)比较工业上合成氨和SO2的催化氧化反应,其生产条件有哪些异同,并解释原因
。
(3)将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中,氨的体积分数为15%,则H2的体积分数为______________。
(4)NH3的用途之一是制造化肥,但在化肥的使用过程中要注意铵态氮肥不可以和草木灰混用,解释其原因 。
(5)NH3是一种重要的化工原料,除了制造化肥之外,再列举出两种NH3的用途
。
科目:高中化学 来源:2011届海南省海口市高三高考调研测试地化学试卷 题型:填空题
(20分)
(I)多项选择题(6分)
下列关于水处理的说法正确的是 。
| A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程 |
| B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度 |
| C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术 |
| D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化 |
 渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜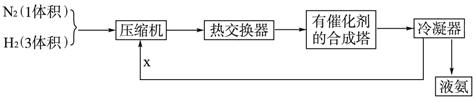
科目:高中化学 来源:2010-2011学年海南省海口市高三高考调研测试地化学试卷 题型:填空题
(20分)
(I)多项选择题(6分)
下列关于水处理的说法正确的是 。
A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程
B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度
C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术
D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化
E.电渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
(II)(14分)
下列是工业合成氨的简要流程示意图:

请回答下列问题:
(1)H2通常用碳氢化合物与水反应,写出有关的反应方程式 ,从冷凝器回流到压缩机中的X是 。
(2)比较工业上合成氨和SO2的催化氧化反应,其生产条件有哪些异同,并解释原因
。
(3)将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中,氨的体积分数为15%,则H2的体积分数为______________。
(4)NH3的用途之一是制造化肥,但在化肥的使用过程中要注意铵态氮肥不可以和草木灰混用,解释其原因 。
(5)NH3是一种重要的化工原料,除了制造化肥之外,再列举出两种NH3的用途
。
科目:高中化学 来源:不详 题型:填空题
| A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程 |
| B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度 |
| C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术 |
| D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化 |
 渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
科目:高中化学 来源: 题型:

科目:高中化学 来源: 题型:阅读理解
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0 ,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)= 。平衡时H2的转化率为 %。
2NH3(g) ΔH<0 ,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)= 。平衡时H2的转化率为 %。
(2)平衡后,若提高H2的转化率,可以采取的措施有 。
A.加了催化剂 B.增大容器体积
C.降低反应体系的温度 D.加入一定量N2
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:
N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
T/ ℃ | 200 | 300 | 400 |
k | K1 | K2 | 0.5 |
请完成下列问题:
① 试比较K1 、K2的大小,K1_______ K2 (填“<”“>”或“=”);
② 下列各项能作为判断该反应达到化学平衡状态的依据是________(填序号字母)
A、容器内N2、H2、NH3的物质的量浓度之比为1:3:2
B、v(N2)正=3 v(H2)逆
C、容器内压强保持不变
D、混合气体的密度保持不变
③400℃时,反应2NH3(g) ![]() N2(g)+3H2(g)的化学平衡常数为_______。当测得NH3、N2和H2的物质的量分别为3mol、2 mol和1 mol时,则该反应的
N2(g)+3H2(g)的化学平衡常数为_______。当测得NH3、N2和H2的物质的量分别为3mol、2 mol和1 mol时,则该反应的
v(N2)正______v(N2) 逆 (填“<”“>”或“=”)。
(4)根据化学反应速率和化学平衡理论,联系合成氨的生产实际,你认为下列说法不正确的是_________。
A、化学反应速率理论可指导怎样在一定时间内快出产品
B、勒夏特列原理可指导怎样使用有限原料多出产品
C、催化剂的使用是提高产品产率的有效方法
D、正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com