
科目:高中化学 来源: 题型:
| ||
科目:高中化学 来源:不详 题型:单选题
| ||
| A.27 | B.18 | C.36 | D.126 |
科目:高中化学 来源:2011-2012学年辽宁省沈阳二中高一(上)月考化学试卷(10月份)(解析版) 题型:选择题
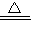 X3(g)+2Y(g),测得生成物组成的混合气体与H2的相对密度为18,则W的相对分子质量为( )
X3(g)+2Y(g),测得生成物组成的混合气体与H2的相对密度为18,则W的相对分子质量为( )科目:高中化学 来源: 题型:单选题
 X3(g)+2Y(g),测得生成物组成的混合气体与H2的相对密度为18,则W的相对分子质量为
X3(g)+2Y(g),测得生成物组成的混合气体与H2的相对密度为18,则W的相对分子质量为科目:高中化学 来源: 题型:
在一定温度下,物质W分解,其反应方程式![]() ,测得生成物组成的混合气体与
,测得生成物组成的混合气体与![]() 的相对密度为18,则W的相对分子质量为 ( )
的相对密度为18,则W的相对分子质量为 ( )
A. 27 B. 18 C. 36 D. 126
科目:高中化学 来源:四川省南山中学2011-2012学年高一下学期期中考试化学试题 题型:058
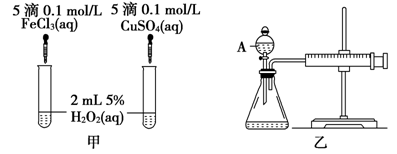
经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验.回答相关问题:

(1)定性分析:如图甲可通过观察________,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是________,写出H2O2在二氧化锰作用下发生反应的化学方程式________.
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略.图中仪器A的名称为________,实验中需要测量的数据是________.检查乙装置气密性的方法是________.
(3)0.6 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,发生如下反应:
2X(g)+Y(g)![]() nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的反应速率为0.1 mol/(L·min),则前2 min内,用X的物质的量浓度变化表示的平均反应速率为________;2 min末时Y的物质的量浓度为________;化学方程式中,Z的化学计量数n=________.
nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的反应速率为0.1 mol/(L·min),则前2 min内,用X的物质的量浓度变化表示的平均反应速率为________;2 min末时Y的物质的量浓度为________;化学方程式中,Z的化学计量数n=________.
(4)在一定温度下,反应:2A(s)+2B(g)![]() C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
A.容器内的压强不随时间而变化
B.混合气的密度不再随时间而变化
C.A的质量不再改变
D.平衡混合气体的平均相对分子质量不再改变
科目:高中化学 来源: 题型:
(10分)经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
(1) 定性分析:如图甲可通过观察____________________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是____________________________________________________________________,
写出H2O2在二氧化锰作用下发生反应的化学方程式
____________________________________________________________________。
(2) 定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为________,实验中需要测量的数据是___________________________________________________________。
检查乙装置气密性的方法是
____________________________________________________________________。
(3) 0.6mol X气体和0.6mol Y气体混合于2 L密闭容器中,发生如下反应:
2X(g)+Y(g)===nZ(g)+2W(g), 2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的反应速率为0.1 mol/(L·min),则前2 min内,用X的物质的量浓度变化表示的平均反应速率为________;2 min末时Y的物质的量浓度为________;化学方程式中,Z的化学计量数n=________。
(4) 在一定温度下,反应:2A(s)+2B(g) C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
A.容器内的压强不随时间而变化
B.混合气的密度不再随时间而变化
C.A的质量不再改变
D.平衡混合气体的平均相对分子质量不再改变
科目:高中化学 来源: 题型:
(10分)经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
(1) 定性分析:如图甲可通过观察____________________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是____________________________________________________________________,
写出H2O2在二氧化锰作用下发生反应的化学方程式
____________________________________________________________________。
(2) 定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为________,实验中需要测量的数据是___________________________________________________________。
检查乙装置气密性的方法是
____________________________________________________________________。
(3) 0.6mol X气体和0.6mol Y气体混合于2 L密闭容器中,发生如下反应:
2X(g)+Y(g)===nZ(g)+2W(g), 2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的反应速率为0.1 mol/(L·min),则前2 min内,用X的物质的量浓度变化表示的平均反应速率为________;2 min末时Y的物质的量浓度为________;化学方程式中,Z的化学计量数n=________。
(4) 在一定温度下,反应:2A(s)+2B(g) C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
A.容器内的压强不随时间而变化
B.混合气的密度不再随时间而变化
C.A的质量不再改变
D.平衡混合气体的平均相对分子质量不再改变
科目:高中化学 来源:四川省期中题 题型:实验题
 C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________ 科目:高中化学 来源: 题型:阅读理解
X、Y、Z三种短周期元素,其单质在常温下都是无色气体,它们的原子序数之和为16。在适当条件下三种单质直接化合,可发生如右图所示变化。已知一个B分子中含有Z元素的原子个数比 C分子中的Z元素的原子个数少一个。
请回答下列问题:
(1)X、Z两元素也可按1:1组合成另一种物质D,D 的电子式为 ,A与C在一定条件下可生成无污染的物质,请写出该反应的化学方程式
(2)X的单质与Z的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。则:正极通入的物质名称是 ;负极电极反应式为 。
(3)X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W溶液吸收生成一种盐。该盐的水溶液pH 7(填“大于”、“小于”或“等于”)其原因是(用离子方程式表示): 。
(4)已知Y的单质与Z的单质生成C的反应是可逆反应,△H<0。将等物质的量的Y、Z的单质充入一密闭容器中,在适当催化剂和恒温,恒压条件下反应。下列说法中,正确的是 (填写下列各项的序号)。
a.达到化学平衡后,再升高温度,C的体积分数增大
b.达到化学平衡时,Y、Z的两种单质在混合气体中的物质的量之比为1:1
c.反应过程,Y的单质体积分数始终为50%
d.达到化学平衡的过程中,混合气体的密度增大
e.达到化学平衡时,正反应速率与逆反应速率相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com