32、某固体混合物可能含有Zn、CaCO
3、Na
2CO
3三种物质,为检测出该混合物中的具体物质及含量,探究小组选择了图中的部分装置,经过实验得知气体产物中含有氢气和二氧化碳.(提示:不考虑稀盐酸的挥发性)
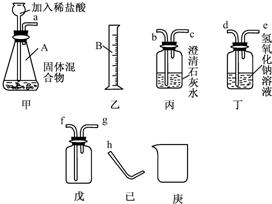
回答下列问题:
(1)装置甲中仪器A的名称是
锥形瓶
,乙中仪器B的名称是
量筒
.
(2)长颈漏斗须伸入液面下的原因是
防止气体从长颈漏斗逸出
.
(3)装置戊若用于排空气法收集某种气体,当气体从g处进入,则可收集到密度比空气
小
的气体(填“大”或“小”).
(4)根据图中所提供的仪器装置,进行合理的连接,可完成以下指定的实验:
①证明该混合物中含有碳酸盐,从左到右的接口顺序为a→
b
.写出除装置甲内的反应外,该项实验中所发生反应的化学方程式:
CO2+Ca(OH)2=CaCO3↓+H2O
.
②证明该混合物中含有锌粉,从左到右接口顺序为a→
b→c→d→e→h
.若在装置气密性良好的情况下,未观察到预期的实验现象,可能的原因是
混合气体中的二氧化碳没有除尽
.
(5)假如固体混合物中不含CaCO
3,在实验中称取m克的样品(允许采用上述装置以外的仪器,但装置甲必须使用),甲同学说可以通过测量氢气体积,然后换算成氢气质量的方法计算出Zn的质量.乙同学说,他也可以用另一种方法获得锌的质量,他的方法是
称出丙、丁装置在反应前后的质量,求出质量差即为CO2的质量;根据CO2的质量可计算出Na2CO3的质量,再由样品质量与Na2CO3的质量可得锌的质量
.