
科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:单选题
| A.①②③④① | B.③④①②① | C.②④①③① | D.②①④③① |
科目:高中化学 来源:2009-2010学年河北省邯郸市高二(下)期末化学试卷(解析版) 题型:选择题
科目:高中化学 来源:09-10年西安临潼区高二下学期期末教学质量检测化学卷 题型:选择题
将淀粉水解,并用新制的Cu(OH)2浊液检验其水解产物的实验中,要进行的主要操作是:①加热;②滴入稀硫酸;③加入新制的Cu(OH)2悬浊液;④加入足量的氢氧化钠溶液.以上各步操作的先后顺序排列正确的是
A.①②③④① B.②①④③① C.②④①③① D.③④①②①
科目:高中化学 来源: 题型:
将淀粉水解,并用新制的Cu(OH)2浊液检验其水解产物的实验中,要进行的主要操作是:①加热;②滴入稀硫酸;③加入新制的Cu(OH)2悬浊液;④加入足量的氢氧化钠溶液.以上各步操作的先后顺序排列正确的是
A.①②③④① B.②①④③① C.②④①③① D.③④①②①
科目:高中化学 来源: 题型:
将淀粉水解,并用新制的Cu(OH)2浊液检验其水解产物的实验中,要进行的主要操作是:①加热;②滴入稀硫酸;③加入新制的Cu(OH)2悬浊液;④加入足量的氢氧化钠溶液.以上各步操作的先后顺序排列正确的是
A.①②③④① B.②①④③① C.②④①③① D.③④①②①
科目:高中化学 来源: 题型:
将淀粉水解,并用新制的Cu(OH)2浊液检验其水解产物的实验中,要进行的主要操作是:①加热;②滴入稀硫酸;③加入新制的Cu(OH)2悬浊液;④加入足量的氢氧化钠溶液.以上各步操作的先后顺序排列正确的是
A.①②③④① B.②①④③① C.②④①③① D.③④①②①
科目:高中化学 来源: 题型:
A.①→②→③→④ B.②→①→④→③
C.②→①→④→③→① D.③→④→①→②→①
科目:高中化学 来源: 题型:阅读理解
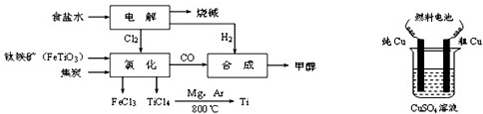
 .
.
| ||
| ||
科目:高中化学 来源: 题型:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com