
现有五种化合物的水溶液(浓度均为1mol/L,各溶液的阴、阳离子均不相同),已知它们的阳离子有K+、Ag+、Ba2+、Fe3+、Al3+,阴离子有OH -、NO3-、SO42-、CO32-、I -,下列关于五种化合物的水溶液说法不正确的是(已知:Fe3+具有较强的氧化性,而I -则具有较强的还原,Fe3+与I -因此而不能大量共存)( )
|
科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:单选题
| A.五种水溶液中一定有K2CO3和AgNO3两种溶液 |
| B.含Ba2+的溶液能与含Fe3+的溶液反应生成两种沉淀 |
| C.含A13+的溶液与含Fe3+的溶液反应后加入淀粉呈蓝色 |
| D.含Al3+的溶液与含Ag+的溶液反应生成白色沉淀 |
科目:高中化学 来源:2012-2013学年浙江省杭州高级中学高一(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源: 题型:阅读理解
小明等同学为了探究酸、碱、盐溶液的导电性,设计了如下实验:
1.在5只250mL烧杯分别加入浓度均为0.1mol·L-1的盐酸、CH3COOH溶液、NaOH溶液、NaCl溶液、氨水各150mL。
2.在5种溶液中分别放入相同规格的石墨电极,按下图连接好。
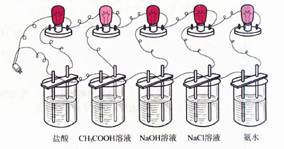
3.接通电源,仔细观察现象。
现象1:五个灯泡都亮起来。
结论: 。
现象2:盐酸、氯化钠、氢氧化钠溶液对应的灯泡较亮,醋酸、氨水对应的灯泡较暗。
结论: 。
思考:
1.酸、碱、盐溶液导电与金属导电的原理是否相同,为什么?
2.同学们为了探究不同电解质之间电离能力的差异,设计了上述实验,通过观察灯泡的明亮程度,判断电解质的电离能力大小,为此必须控制其他能影响灯泡亮度的一些因素,使之保持一致,从而不影响灯泡的明亮程度。在本实验中,采取了哪些主要措施来控制其他因素对灯泡亮度的影响?(写出三条即可) 。
3.小明同学根据现象2得出一个结论:氯化氢、氯化钠、氢氧化钠是强电解质,醋酸、一水合氨是弱电解质。你同意他这个观点吗?为什么?
。
4.为了进一步探究氯化氢等化合物是强电解质,小红同学在老师的帮助下测定了0.1mol·L-1的盐酸中的氢离子浓度,通过对结果的分析,即可得出结论。说明氯化氢是强电解质的理由是:测得溶液中的氢离子浓度 0.1mol·L-1(选填>、<、=)。
5.同学们在实验的基础上,进一步查阅资料得知:一般来说, 是强电解质, 是弱电解质。根据以上结论推测:如果将上述实验中的醋酸和氨水混匀,然后分别盛放在原来的烧杯中。接通电源,可以观察到的现象是:
A.与混合前无任何区别。
B.5只灯泡都亮起来,亮度完全相同。
C.只有盐酸、氯化钠、氢氧化钠溶液对应的灯泡亮起来,另外两只不亮。
D.5个灯泡都亮起来,盐酸、氯化钠、氢氧化钠溶液对应的灯泡较亮,另外两只略暗,但明显比混合前明亮。
科目:高中化学 来源: 题型:
科目:高中化学 来源: 题型:
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3- NO3- OH- |
科目:高中化学 来源:不详 题型:问答题
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3- NO3- OH- |
科目:高中化学 来源:2012年河北省衡水中学高考化学三模试卷(解析版) 题型:解答题
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3- NO3- OH- |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com