
如图所示的实验原理、方法、装置或操作正确的是( )
|
科目:高中化学 来源:不详 题型:单选题
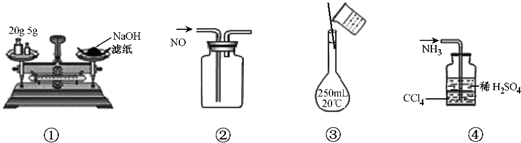
| A.①称量氢氧化钠固体 |
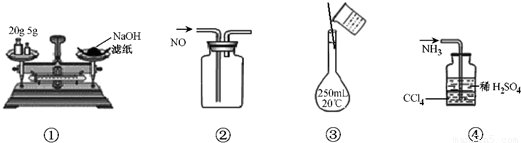
| B.②收集NO气体 |
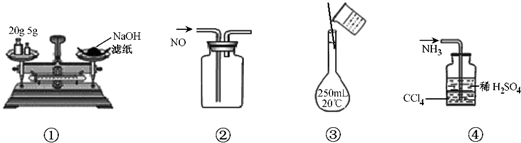
| C.③配制100mL0.10mol?L-1盐酸 |
| D.④吸收NH3不会造成倒吸 |
科目:高中化学 来源:2011年浙江省宁波市余姚中学高考化学二模试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源:同步题 题型:实验题


科目:高中化学 来源:物理教研室 题型:058

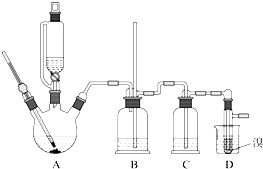
(1)玻璃管E内发生反应的化学方程式______________.
(2)小试管C的作用是_______________.
(3)广口瓶D内盛的试剂是____________.装置D的三个主要作用是____________.
(4)从试管E导出气体成分是______________.
(5)装置F中U形管所收集的物质的颜色、状态是______________.
(6)若U形管内收集到的物质很少,分析其原因,不可能的是_________(填标号)
a.装置气密性不好
b.制得的SO2中混有少量H2S杂质使催化剂中毒
c.气体流速过快
(7)以U形管导出的尾气的处理方法是_______________.
考查考生对物质鉴别方法的一般原则和原理的理解及应用能力.
科目:高中化学 来源: 题型:阅读理解
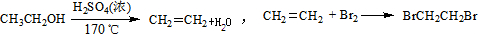
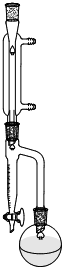
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g?cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
科目:高中化学 来源: 题型:阅读理解
| H2SO4、134~135℃ |
| H2SO4 |
| 135℃ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com