
常温下,0.1mol/L的一元酸HA溶液其pH>1,而0.1mol/L的一元碱BOH的溶液中c(OH-)/c(H+)=1012,将此两种溶液等体积混合后,所得溶液中离子浓度大小关系正确的是( )
|
科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:单选题
| A.c(OH-)>c(H+)>c(B+)>c(A-) | B.c(OH-)<c(H+)<c(A-)<c(B+) |
| C.c(H+)<c(OH-)<c(A-)<c(B+) | D.c(OH-)=c(H+)>c(B+)=c(A-) |
科目:高中化学 来源:2010-2011学年辽宁省营口市高二(上)期末化学试卷(解析版) 题型:选择题
科目:高中化学 来源:0119 同步题 题型:填空题
 ,据此完成下列问题:
,据此完成下列问题: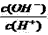 的值____________ (填:增大、不变、减小)
的值____________ (填:增大、不变、减小) 科目:高中化学 来源: 题型:
| 实验编号 | HA | NaOH | 混合溶液的pH |
| 甲 | C(HA)=0.2mol?L-1 | C(NaOH)=0.2mol?L-1 | pH=a |
| 乙 | C(HA)=c1 mol?L-1 | C(NaOH)=0.2mol?L-1 | pH=7 |
| 丙 | C(HA)=0.1mol?L-1 | C(NaOH)=0.1mol?L-1 | pH=9 |
| 丁 | pH=2 | pH=12 | pH=b |
科目:高中化学 来源: 题型:
(14分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | HA | NaOH | 混合溶液的pH |
| 甲 | C(HA)=0.2 mol·L-1 | C(NaOH)=0.2mol·L-1 | pH=a |
| 乙 | C(HA)=c1 mol·L-1 | C(NaOH)=0.2mol·L-1 | pH=7 |
| 丙 | C(HA)=0.1 mol·L-1 | C(NaOH)=0.1mol·L-1 | pH=9 |
| 丁 | pH=2 | pH=12 | pH=b |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸? 。
(2)若考虑其他组的实验结果,则c1 (填“<”、“>”或“=”)0.2 mol·L-1;乙组实验中HA和NaOH溶液混合前,HA溶液中C(A-)与NaOH溶液中C(Na+)的关系是 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 ;其中,C(A-)= mol·L-1(不能做近似计算,回答准确值,结果不一定要化简)。
(4)丁组实验中,HA和NaOH溶液混合前C(HA) (填“<”、“>”或“=”)C(NaOH); b 7(填“<”、“>”或“=”)
科目:高中化学 来源:2011-2012学年浙江东阳中学、兰溪一中高二下学期期中考试化学卷(带解析) 题型:填空题
(14分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | HA | NaOH | 混合溶液的pH |
| 甲 | C(HA)=0.2 mol·L-1 | C(NaOH)=0.2mol·L-1 | pH=a |
| 乙 | C(HA)=c1 mol·L-1 | C(NaOH)=0.2mol·L-1 | pH=7 |
| 丙 | C(HA)="0.1" mol·L-1 | C(NaOH)=0.1mol·L-1 | pH=9 |
| 丁 | pH=2 | pH=12 | pH=b |
科目:高中化学 来源:2013届浙江东阳中学、兰溪一中高二下学期期中考试化学卷(解析版) 题型:填空题
(14分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
|
实验编号 |
HA |
NaOH |
混合溶液的pH |
|
甲 |
C(HA)=0.2 mol·L-1 |
C(NaOH)=0.2mol·L-1 |
pH=a |
|
乙 |
C(HA)=c1 mol·L-1 |
C(NaOH)=0.2mol·L-1 |
pH=7 |
|
丙 |
C(HA)=0.1 mol·L-1 |
C(NaOH)=0.1mol·L-1 |
pH=9 |
|
丁 |
pH=2 |
pH=12 |
pH=b |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸? 。
(2)若考虑其他组的实验结果,则c1 (填“<”、“>”或“=”)0.2 mol·L-1;乙组实验中HA和NaOH溶液混合前,HA溶液中C(A-)与NaOH溶液中C(Na+)的关系是 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 ;其中,C(A-)= mol·L-1(不能做近似计算,回答准确值,结果不一定要化简)。
(4)丁组实验中,HA和NaOH溶液混合前C(HA) (填“<”、“>”或“=”)C(NaOH); b 7(填“<”、“>”或“=”)
科目:高中化学 来源:2012-2013学年浙江省兰溪一中、东阳中学联考高二(下)期中化学试卷(解析版) 题型:填空题
| 实验编号 | HA | NaOH | 混合溶液的pH |
| 甲 | C(HA)=0.2mol?L-1 | C(NaOH)=0.2mol?L-1 | pH=a |
| 乙 | C(HA)=c1 mol?L-1 | C(NaOH)=0.2mol?L-1 | pH=7 |
| 丙 | C(HA)=0.1mol?L-1 | C(NaOH)=0.1mol?L-1 | pH=9 |
| 丁 | pH=2 | pH=12 | pH=b |
科目:高中化学 来源:2012-2013学年浙江省兰溪一中、东阳中学联考高二(下)期中化学试卷(解析版) 题型:填空题
| 实验编号 | HA | NaOH | 混合溶液的pH |
| 甲 | C(HA)=0.2mol?L-1 | C(NaOH)=0.2mol?L-1 | pH=a |
| 乙 | C(HA)=c1 mol?L-1 | C(NaOH)=0.2mol?L-1 | pH=7 |
| 丙 | C(HA)=0.1mol?L-1 | C(NaOH)=0.1mol?L-1 | pH=9 |
| 丁 | pH=2 | pH=12 | pH=b |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com