
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41kJ/mol相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:
| ||||||||||||||||||||||||||
科目:高中化学 来源: 题型:
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
科目:高中化学 来源:西城区一模 题型:单选题
| 容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系 能量的变化 | |||
| CO | H2O | CO2 | H2 | ||
| ① | 1 | 4 | 0 | 0 | 放出热量:32.8 kJ |
| ② | 0 | 0 | 1 | 4 | 热量变化:Q |
| A.容器①中反应达平衡时,CO的转化率为80% |
| B.容器①中CO的转化率等于容器②中CO2的转化率 |
| C.平衡时,两容器中CO2的浓度相等 |
| D.容器①中CO反应速率等于H2O的反应速率 |
科目:高中化学 来源:2010-2011学年湖北省襄樊市四校高二(上)期中化学试卷(解析版) 题型:解答题
 molCO2、
molCO2、 molH2,欲使反应达平衡时CO的转化率与(1)相同,则还需满足的条件是______;
molH2,欲使反应达平衡时CO的转化率与(1)相同,则还需满足的条件是______;科目:高中化学 来源:2013年北京市西城区高考化学一模试卷(解析版) 题型:选择题
| 容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系 能量的变化 | |||
| CO | H2O | CO2 | H2 | ||
| ① | 1 | 4 | 放出热量:32.8 kJ | ||
| ② | 1 | 4 | 热量变化:Q | ||
科目:高中化学 来源:不详 题型:问答题
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |

科目:高中化学 来源:不详 题型:问答题
科目:高中化学 来源: 题型:
(2013?西城区一模)已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41kJ/mol相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:
| ||||||||||||||||||||||
科目:高中化学 来源: 题型:
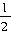 O2(g)=H2O(g);ΔH=-241.8kJ/mol
O2(g)=H2O(g);ΔH=-241.8kJ/mol科目:高中化学 来源: 题型:
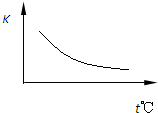 工业上制备H2的一种重要方法是:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q kJ?mol-1.已知该反应的平衡常数K与温度的关系如图所示.若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质的浓度(mol?L-1)随时间的变化关系如下表:
工业上制备H2的一种重要方法是:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q kJ?mol-1.已知该反应的平衡常数K与温度的关系如图所示.若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质的浓度(mol?L-1)随时间的变化关系如下表:| Kt℃ 时间/min |
CO(g) | H2O(g) | CO2(g) | H2(g) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c4 |
| 4 | c1 | c2 | c3 | c4 |
科目:高中化学 来源:2013-2014学年重庆市高三上学期12月月考理综化学试卷(解析版) 题型:选择题
已知:CO(g)+H2O(g)=CO2(g)+H2(g)△H=﹣41kJ/mol相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:
|
容器 编号 |
起始时各物质物质的量/mol |
达平衡过程体系 |
|||
|
CO |
H2O |
CO2 |
H2 |
能量的变化 |
|
|
① |
1 |
4 |
0 |
0 |
放出热量:32.8 kJ |
|
② |
0 |
0 |
1 |
4 |
热量变化:Q |
下列说法中,不正确的是( )
A.容器①中反应达平衡时,CO的转化率为80%
B.容器②中吸收的热量O为32.8 kJ
C.平衡时,两容器中CO2的浓度相等
D.容器①中当CO反应速率等于H2O的反应速率时,反应可能达到平衡
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com