
纯碱溶于水中会发生水解反应,使溶液中OH-的个数比H+的多.下列说法不正确的是( )
|
科目:初中化学 来源:不详 题型:单选题
| A.Na2CO3溶液显碱性,可使无色酚酞试液变红色 |
| B.向Na2CO3溶液中加入适量的NaOH可抑制Na2CO3水解反应的进行 |
| C.可用稀盐酸来判断Na2CO3溶液中是否含NaOH |
| D.可用食醋来区别纯碱和NaOH |
科目:初中化学 来源:2006年第十六届“天原杯”全国初中学生化学素质和实验能力竞赛(湖北赛区)初赛试卷(解析版) 题型:选择题
科目:初中化学 来源: 题型:单选题
科目:初中化学 来源: 题型:阅读理解
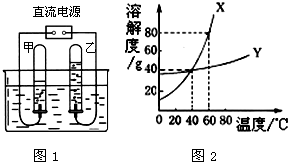 水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:
水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:| 感官指标 | 化学指标 | 细菌指标 |
| 水质无色无味澄清 | PH:6.5~8.5 | 细菌总个数<100个/mL等 |
科目:初中化学 来源: 题型:解答题
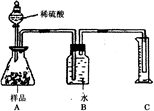 烧碱是常用的消毒剂,因烧碱价廉而被广泛地应用,工业烧碱中常常因含有Na2CO3杂质而不纯.甲、乙两同学设计实验来探究工业烧碱中NaOH的质量分数.
烧碱是常用的消毒剂,因烧碱价廉而被广泛地应用,工业烧碱中常常因含有Na2CO3杂质而不纯.甲、乙两同学设计实验来探究工业烧碱中NaOH的质量分数.科目:初中化学 来源: 题型:
 27、利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究:
27、利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究:| 实验操作 | 实验现象 | 实验结论 | |
| ① | 取少量滤液,滴入纯碱溶液 | 没有白色沉淀产生 | |
| ② | 另取少量滤液,滴入,静置. | 含有碳酸钠 和氢氧化钠 |
科目:初中化学 来源: 题型:阅读理解
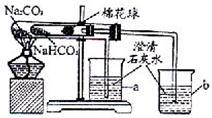 27、某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质后,联想到家中蒸制馒头时常用的物质小苏打(NaHCO3),于是采用市售的小苏打样品进行了如下实验探究.
27、某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质后,联想到家中蒸制馒头时常用的物质小苏打(NaHCO3),于是采用市售的小苏打样品进行了如下实验探究.科目:初中化学 来源: 题型:
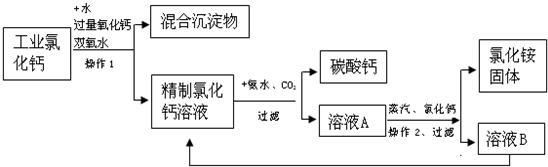
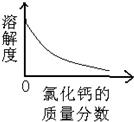
科目:初中化学 来源: 题型:阅读理解
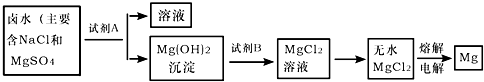
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com