

科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
烷烃的系统名称分四个部分:
①主链名称 ②取代基名称 ③取代基位置 ④取代基数目.
这四部分在烷烃命名规则中的先后顺序是
查看答案和解析>>
科目: 来源: 题型:解答题
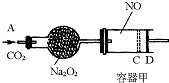 如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的
如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的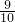 ,随着CO2的继续通入,活塞又逐渐向右移动.(不考虑活塞的磨擦)
,随着CO2的继续通入,活塞又逐渐向右移动.(不考虑活塞的磨擦)查看答案和解析>>
科目: 来源: 题型:解答题
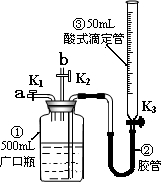
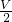 时,则广口瓶①的气体体积为______;
时,则广口瓶①的气体体积为______;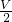 ,则通入氧气的体积可能为______.
,则通入氧气的体积可能为______.查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题

查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:多选题
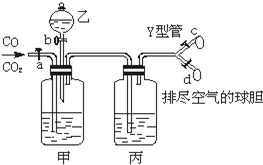 下图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y型管和止水夹分别接c、d两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙分别盛放的溶液是
下图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y型管和止水夹分别接c、d两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙分别盛放的溶液是查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com