
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
用Na2CO3固体配制1mol/L的Na2CO3溶液100mL.
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③100mL量筒;④100mL容量瓶;⑤250mL量筒;⑥托盘天平;⑦50mL烧杯;⑧药匙;应选用的仪器(填编号)______.
(2)应称取Na2CO3的质量为______.
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
 CaSiO3+CO2↑,SiO2 和CaSiO3 均为固体)
CaSiO3+CO2↑,SiO2 和CaSiO3 均为固体)查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
| 选项 | 实验操作和现象 | 预期实验目的或结论 |
| A | 用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色 | 说明该食盐试样不含KIO3 |
| B | 银氨溶液中滴入少量组成为C2H4O2的液态有机物,水浴微热,有银镜出现. | 可确定该有机物一定是甲酸甲酯 |
| C | 向两支盛有KI3的溶液的试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀. | KI3溶液中存在平衡: I3-?I2+I- |
| D | 室温下向CuCl2和少量FeCl3的混合溶液中,加入铜屑,充分搅拌,过滤,得蓝绿色溶液. | 除去杂质FeCl3得纯净CuCl2溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
 4NO+6H2O,4NO+3O2+2H2O→4HNO3
4NO+6H2O,4NO+3O2+2H2O→4HNO3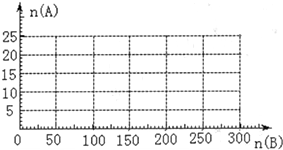
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com