
科目: 来源:2012-2013学年北京市东城区普通校高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年北京市东城区普通校高三(上)期中化学试卷(解析版) 题型:选择题
| 操作 | 现象 | 结论 | |
| A | 用CH3COOH溶液浸泡水垢 | 水垢溶解,有无色气泡 | 碱性:NaHCO3>CH3COONa |
B | 测定等浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 向FeBr2溶液中通入过量Cl2 | 溶液由浅绿色变成黄色 | 氧化性:Br2>Fe3+ |
| D | 向盛有1mL 0.1mol?L-1 AgNO3溶液的试管中滴加2~4滴0.1mol?L-1 NaCl溶液,后继续滴加 0.1mol?L-1 KI溶液. | 出现黄色沉淀 | 溶解度:AgCl>AgI |
查看答案和解析>>
科目: 来源:2012-2013学年北京市东城区普通校高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年北京市东城区普通校高三(上)期中化学试卷(解析版) 题型:解答题

查看答案和解析>>
科目: 来源:2012-2013学年北京市东城区普通校高三(上)期中化学试卷(解析版) 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g | h | ||
| 4 | J | k |
查看答案和解析>>
科目: 来源:2012-2013学年北京市东城区普通校高三(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2012-2013学年北京市东城区普通校高三(上)期中化学试卷(解析版) 题型:解答题
| 组别 | 一元酸 | NaOH | 混合溶液的pH |
| 甲 | c(HX)=0.1mol/L | c(NaOH)=0.1mol/L | pH=a |
| 乙 | c(HY)=c1 mol/L | c(NaOH)=0.1mol/L | pH=7 |
| 丙 | c(HZ)=0.1mol/L | c(NaOH)=0.1mol/L | pH=9 |
| 丁 | pH=2 HZ | pH=12 NaOH | pH=b |
查看答案和解析>>
科目: 来源:2012-2013学年北京市东城区普通校高三(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2012-2013学年北京市东城区普通校高三(上)期中化学试卷(解析版) 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |

查看答案和解析>>
科目: 来源:2011-2012学年云南省大理州云龙一中高二(上)期末化学试卷(解析版) 题型:选择题
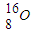 与
与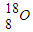
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com