相关习题
0 64593 64601 64607 64611 64617 64619 64623 64629 64631 64637 64643 64647 64649 64653 64659 64661 64667 64671 64673 64677 64679 64683 64685 64687 64688 64689 64691 64692 64693 64695 64697 64701 64703 64707 64709 64713 64719 64721 64727 64731 64733 64737 64743 64749 64751 64757 64761 64763 64769 64773 64779 64787 203614
科目:
来源:2012-2013学年福建省福州市福清市东张中学高二(上)期中化学试卷(理科)(解析版)
题型:选择题
已知448℃时反应H
2(g)+I
2(g)?2HI(g)的平衡常数是49,则HI(g)?

H
2(g)+

I
2(g)在该温度下的平衡常数是( )
A.
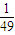
B.2401
C.7
D.

查看答案和解析>>
科目:
来源:2012-2013学年福建省福州市福清市东张中学高二(上)期中化学试卷(理科)(解析版)
题型:选择题
未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且有些可以再生.下列属最有希望的新能源的是( )
①天然气 ②煤 ③核能 ④水电 ⑤太阳能 ⑥燃料电池 ⑦风能 ⑧氢能.
A.①②③④
B.⑤⑥⑦⑧
C.③④⑤⑥
D.除①②外
查看答案和解析>>
科目:
来源:2012-2013学年福建省福州市福清市东张中学高二(上)期中化学试卷(理科)(解析版)
题型:选择题
在反应:2A+B?3C+4D中,所表示的反应速率最快的是( )
A.v(A)=0.4mol?L-1?s-1
B.v(B)=0.3mol?L-1?s-1
C.v(C)=1.2mol?L-1?s-1
D.v(D)=0.8mol?L-1?s-1
查看答案和解析>>
科目:
来源:2012-2013学年福建省福州市福清市东张中学高二(上)期中化学试卷(理科)(解析版)
题型:选择题
电解饱和食盐水,当阴极附近有0.4molOH-生成时,阳极生成( )
A.0.2molH2
B.0.2molCl2
C.0.4molH2
D.0.4molCl2
查看答案和解析>>
科目:
来源:2012-2013学年福建省福州市福清市东张中学高二(上)期中化学试卷(理科)(解析版)
题型:解答题
已知下列热化学方程式:Zn(s)+1/2O2(g)=ZnO(s)△H=-351.1kJ/molHg(l)+1/2O2(g)=HgO(s)△H=-90.7kJ/mol由此可知反应 Zn(s)+HgO(s)=ZnO(s)+Hg(l) 的焓变为______.
查看答案和解析>>
科目:
来源:2012-2013学年福建省福州市福清市东张中学高二(上)期中化学试卷(理科)(解析版)
题型:解答题
氢氧燃料电池是最常见的燃料电池,该电池在正极通入氧气,在负极通入氢气,而电解质溶液通常是KOH溶液.
(1)请写出氢氧燃料电池的正极反应方程式.
(2)氢氧燃料电池有何优点?
查看答案和解析>>
科目:
来源:2012-2013学年福建省福州市福清市东张中学高二(上)期中化学试卷(理科)(解析版)
题型:解答题
A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol/L.反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L.则2min内反应的平均速率VA=______,VB=______,VC=______.该反应的化学反应方程式为______.
查看答案和解析>>
科目:
来源:2012-2013学年福建省福州市福清市东张中学高二(上)期中化学试卷(理科)(解析版)
题型:解答题
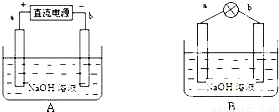
某兴趣小组采用如下方法制作氢氧燃料电池.
(1)如图A所示:a、b均为多孔石墨棒(多孔石墨棒,可吸附并储存生成的气体),其中a与直流电源正极相连,b与直流电源负极相连,电解质溶液为NaOH溶液,则a电极上发生的电极反应式为______,电解后溶液的pH______(填“增大”、“减小”或“不变”).
(2)然后如图B所示,移走直流电源,在a、b极间连接一个发光二极管,可以看到二极管发光.此时的电流方向是______(填“a→b”或“b→a”),b极的电极反应式为______.
(3)假设a极吸收22.4L(标准状况)气体,能量转化率为60%,则通过二极管的电子的物质的量为______.
查看答案和解析>>
科目:
来源:2012-2013学年福建省福州市福清市东张中学高二(上)期中化学试卷(理科)(解析版)
题型:解答题
PCl5的热分解反应如下:PCl5(g)?PCl3(g)+Cl2(g)
(1)写出反应的平衡常数表达式;
(2)已知某温度下,在容积为10.0L的密闭容器中充入2.00mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150mol/L.计算该温度下的平衡常数.
查看答案和解析>>

 H2(g)+
H2(g)+ I2(g)在该温度下的平衡常数是( )
I2(g)在该温度下的平衡常数是( )