
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:选择题
为鉴定某盐成分,选用如下方法:下列结论正确的是( )
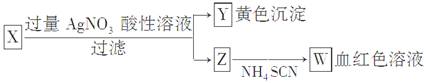
A.Z中一定有Fe3+ B.X中一定有Fe2+
C.Y为AgBr沉淀 D.X一定为FeBr2
查看答案和解析>>
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:选择题
2008年9月27日16时41分,航天员翟志刚身着“飞天”航天服出舱活动,茫茫太空中第一次留下中国人的足迹。“飞天”舱外航天服是我国自行研制的,使用了多种新材料。下列对材料的说法错误的是( )
A.新材料的开发和应用,是社会发展和人类进步的一种标志
B.水泥、玻璃、陶瓷属于新型无机非金属材料
C.传统的无机非金属材料虽有不少优点,但质脆、经不起热冲击
D.新型结构陶瓷具有承受高温、抗氧化、耐磨损、密度小等特点,可应用于宇航事业
查看答案和解析>>
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:选择题
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C2AlN+3CO下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为-3
D.氮化铝晶体属于分子晶体
查看答案和解析>>
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:选择题
我国计划用8年时间对5·12四川汶川大地震进行灾后重建,重建需要大量钢材和金属合金材料。下列说法正确的是( )
A.铁和钢材的主要化学成分相同,性质也相同
B.硬铝(AlCuMgMnSi合金)可用于制造耐高温门窗
C.黄铜矿(CuFeS2)可冶炼出Cu、Fe,同时可制取硫酸
D.铁矿石是一种可再生资源,没有必要进行开采限制
查看答案和解析>>
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:选择题
下列有关铁及其化合物的说法中不正确的是( )
A.分别还原a mol Fe2O3所需H2、Al、CO物质的量之比为3 ∶2 ∶3
B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4
C.工业上可用铁制容器储存、运输浓硝酸、浓硫酸
D.检验某物质是否含Fe2O3的操作步骤为:样品→粉碎→加热→溶解→过滤→向滤液中加KSCN溶液
查看答案和解析>>
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:选择题
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水的离子反应是4FeO42-+10H2O===4Fe(OH)3(胶体)+3O2↑+8OH-,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入一定量的KOH就可制得高铁酸钾。制备高铁酸钠的两种方法的主要反应原理如下:
湿法制备:2Fe(OH)3+3ClO-+4OH-===2FeO42-+3Cl-+5H2O;
干法制备:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑。
下列有关说法中错误的是( )
A.高铁酸钾与水反应时,水发生氧化反应
B.干法中每生成1 mol Na2FeO4共转移4 mol电子
C.湿法中每生成1 mol Na2FeO4共转移3 mol电子
D.K2FeO4处理水时,不仅能杀菌,并使悬浮杂质沉降
查看答案和解析>>
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:选择题
某化学兴趣小组用回收的镁铝合金制取氢气。现有10.8 g镁铝合金,下列说法正确的是( )
A.常温下与足量18 mol·L-1 H2SO4溶液反应,最多可放出0.6 mol H2
B.常温下与足量2 mol·L-1 HNO3溶液反应,最少可放出0.45 mol H2
C.常温下与足量2 mol·L-1 H2SO4溶液反应,放出H2的物质的量在0.45 mol~0.6 mol之间
D.常温下与足量2 mol·L-1 NaOH溶液反应,放出H2的物质的量在0.45 mol~0.6 mol之间
查看答案和解析>>
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:选择题
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物足量溶液A充分反应测定生成气体的体积;
方案Ⅱ:铜铝混合物足量溶液B充分反应测定剩余固体的质量
下列有关判断中不正确的是( )
A.溶液A和B均可以是盐酸或NaOH溶液
B.若溶液B选用浓硝酸,则测得铜的质量分数偏小
C.溶液A和B均可选用稀硝酸
D.实验室中方案Ⅱ更便于实施
查看答案和解析>>
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:填空题
现有浓度分别为1 mol/L的FeCl3、FeCl2、CuCl2混合溶液100 mL,加入一定量的铁粉,按下列情况填空。
(1)充分反应后,如果溶液中还有一定量的Cu2+,则溶液中一定含有的金属离子还有________,该离子在溶液中的物质的量范围为________,可能含有的金属或金属离子为________。
(2)反应完毕后,铁粉有剩余,溶液中一定含有的金属离子为________,为________mol,一定没有的金属离子为________。
查看答案和解析>>
科目: 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:实验题
(9分)由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去):
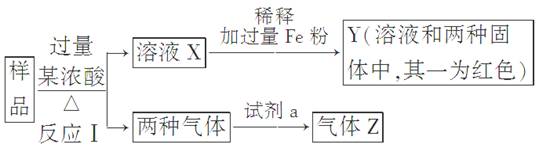
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填写化学式)________。
(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是____________________________________________________________
________________________________________________________________________。
②若Z为两种气体的混合物,试剂a为适量水,则Z中两种气体的化学式是________。
(3)向Y中通入过量氯气,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)________。
(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈蓝色并有红褐色沉淀生成。当消耗2 mol I-时,共转移3 mol电子,该反应的离子方程式是________。
(5)另取原样品,加入足量稀硫酸充分反应。若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中的物质用化学式表示)________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com