
科目: 来源:2011-2012学年北京四中高二(上)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2011-2012学年北京四中高二(上)期末化学试卷(解析版) 题型:填空题
查看答案和解析>>
科目: 来源:2011-2012学年北京四中高二(上)期末化学试卷(解析版) 题型:解答题
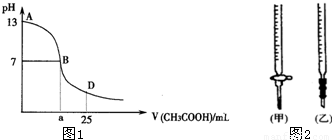
| 锥形瓶中溶液 | 滴定管 中溶液 | 选用 指示剂 | 选用 滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
查看答案和解析>>
科目: 来源:2011-2012学年北京四中高二(上)期末化学试卷(解析版) 题型:填空题
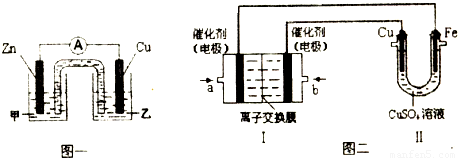
查看答案和解析>>
科目: 来源:2011-2012学年北京四中高二(上)期末化学试卷(解析版) 题型:填空题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡时数据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | akJ | bkJ | ckJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
查看答案和解析>>
科目: 来源:2012-2013学年甘肃省武威三中高二(上)期中化学试卷(文科)(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年甘肃省武威三中高二(上)期中化学试卷(文科)(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年甘肃省武威三中高二(上)期中化学试卷(文科)(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com