
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:选择题
表示下列变化的化学用语中,正确的是
A. 碳酸氢钠溶液与少量澄清石灰水反应的离子方程式:
HCO- 3+Ca2++OH‑ == CaCO3↓+H2O
B. 氯化铵与氢氧化钠两种浓溶液混合加热:OH-+ NH+ 4  H2O+NH3↑
H2O+NH3↑
C. NaHCO3的水解:HCO- 3+H2O == H3O++CO2- 3
D. 钢铁吸氧腐蚀的正极反应:4OH- →O2↑+2H2O+4e-
查看答案和解析>>
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:选择题
对下列各溶液中,微粒的物质的量浓度关系表述正确的是
A. 某溶液中存在的离子只有Cl-、OH-、NH4+、H+,该溶液中离子浓度大小关系可能为c(Cl-)>c(NH4+) >c(OH-)>c(H+)
B. 0.1 mol·L-1(NH4)2SO4溶液中:c(H+)>c(NH4+)
C. 0.1 mol·L-1的HCl溶液与0.1 mol·L-1的NaOH溶液等体积混合:
c(H+) +c(Na+)== c (OH-)+c(Cl-)
D. 0.1 mol·L-1 CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:选择题
关于下列图示的说法中,正确的是
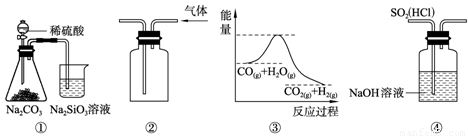
A. 图①所示实验可比较硫、碳、硅三种元素的非金属性强弱
B. 用图②所示实验装置排空气法收集CO2气体
C. 图③表示可逆反应CO(g)+H2O(g)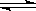 CO2(g)+H2(g)的ΔH大于0
CO2(g)+H2(g)的ΔH大于0
D. 图④装置可以用来除去SO2中的HCl
查看答案和解析>>
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:选择题
已知Co2O3在酸性溶液中易被还原成Co2+,且Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列叙述中,正确的是
A. Cl2通入FeI2溶液中,可存在反应3Cl2+6FeI2==2FeCl3+4FeI3
B. 每1 mol Co2O3在酸性溶液中被氧化生成Co2+时转移2 mol e-
C. FeCl3溶液能使淀粉—KI试纸变蓝
D. I2是ⅦA族元素单质,具有较强的氧化性,可以将Co2+氧化成Co2O3
查看答案和解析>>
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:选择题
已知,常温下,KSP (AgCl)=1.8×10-10 mol2·L-2,KSP(AgI)=8.3×10-17 mol2·L-2,下列叙述中,正确的是
A. 常温下,AgCl在饱和NaCl溶液中的 KSP 比在纯水中的 KSP小
B. 向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色
C. 将0.001 mol·L-1的AgNO3 溶液滴入KCl和KI的混合溶液中,一定先产生AgI沉淀
D. 向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-)
查看答案和解析>>
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:实验题
(5分)(1) 化学是一门以实验为基础的学科,下列实验操作的描述中,正确的是_______________(填序号)。
① 为使稀硫酸和锌制取氢气的速率加快,可向稀硫酸中加入用铜丝网包裹的锌粒
② 用托盘天平称取10.4 g食盐时,将食盐放在右盘中的纸片上称量
③ 配制一定物质的量浓度的溶液时,容量瓶洗涤后未进行干燥[来源:Z_xx_k.Com]
④ 以酚酞作指示剂,用标准浓度的盐酸滴定NaOH溶液,待溶液变成浅红色时即停止滴定
⑤ 测定溶液的pH时,用洁净、干燥的玻璃棒蘸取待测溶液,点在试纸中部,待变色后与标准比色卡对照读数
(2) 下列说法中,符合安全要求的是__________(填序号)。
① 在通风橱内做铜与浓硝酸反应的实验
② 实验中剩余的过氧化钠粉末用纸包裹好后,放入垃圾桶内
③ 闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔
④ 为了节约时间,锌与稀硫酸反应一开始有氢气放出,就直接做氢气点燃实验
查看答案和解析>>
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:实验题
(15分)某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)。

请回答下列问题:
(1) A中发生反应的化学方程式为_______________________________________。
(2) 各装置的正确连接顺序为(填写装置代号)A→______→______→______→
______D。
(3) 装置C的作用是________________________________________________,
写出装置D中反应的离子方程式____________________________________。
(4) 反应开始后,B中硬质玻璃管内的现象为______________________________;
可以检验生成物中含有Fe3+的试剂是____________(填写试剂名称)。
(5) 该小组欲用下图所示装置收集尾气,并测量多余气体的体积。

① 若如图所示量气装置由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是________(填“酸式”或“碱式”)滴定管。
② 为提高测量的准确性,上图装置中的液体可用________,
收集完气体后,读数前应进行的操作是____________。
③ 如果开始读数时操作正确,最后读数时俯视右边滴定管液面,会导致所测气体的体积__________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:填空题
(11分 )A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;
D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。
请回答下列问题:
(1) X的化学式为______,D的原子结构示意图为______。
(2) 元素的非金属性C______E(填“>”、“<”或“=”),下列各项中,能说明这一结论的事实有______(填序号)。
① 氢化物H2E的酸性比H2C强
② 氢化物H2C的热稳定性比H2E强
③ 氢化物H2E的水溶液放置在空气中会变浑浊
(3) 将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。

已知(ⅰ) 浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC。
(ⅱ) NaOH溶液与BC2反应的化学方程式为:
2NaOH+2BC2==NaBC2+NaBC+H2O
NaOH溶液与BC气体不反应
a. 装置①、②、③中盛放的药品依次是______、______、______。
b. 通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是______(填一种气体的化学式)。
c. 能够说明实验已成功的现象是___________________________。
查看答案和解析>>
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:填空题
(7分)下图各物质是中学化学中常见的物质,甲、乙均是离子化合物,且阴、阳离子个数比为1∶1。甲是发酵粉的主要成分,乙是一种常用的化肥。B、D常温常压下是气体。请回答下列问题:
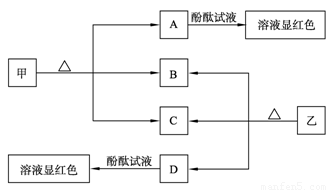
(1) 甲的俗名是____________________________。
(2) A、D物质的水溶液分别滴入酚酞试液后,溶液均显红色,说明溶液均显性,其原理是否相同?请用必要的文字加以解释并写出离子方程式:
__________________________________________________________。
(3) 向饱和氯化钠溶液中通入气体D至饱和后,再通入足量的气体B可制得物质甲,写出该反应的化学方程式:__________________________________________。
查看答案和解析>>
科目: 来源:2010-2011学年山东省济南市高三教学质量调研(一模)化学试卷 题型:填空题
(17分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g) 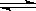 CH3OH(g)。
CH3OH(g)。
(1) 分析该反应并回答下列问题:
① 平衡常数表达式为K= 。
② 下列各项中,不能够说明该反应已达到平衡的是______________(填序号)。
a. 恒温、恒容条件下,容器内的压强不发生变化
b. 一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c. 一定条件下,CO、H2和CH3OH的浓度保持不变
d. 一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2) 下图是该反应在不同温度下CO的转化率随时间变化的曲线。
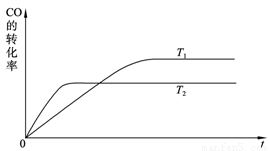
① 该反应的焓变ΔH____________0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1____________K2(填“>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是______________。
a. 升高温度b. 将CH3OH(g)从体系中分离
c. 使用合适的催化剂d. 充入He,使体系总压强增大
(3) 已知在常温常压下:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)ΔH =-a kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g) ΔH =-b kJ·mol-1
③ H2O(g)= H2O(l) ΔH=-c kJ·mol-1
则,CH3OH(l)+O2(g) =CO(g)+2H2O(l) ΔH=______________kJ·mol-1。
(4) 2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。

① 该电池工作时,b口通入的物质为____________, c口通入的物质为__________。
② 该电池正极的电极反应式为:_______________________________。
③ 工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有___________NA个电子转移。

(5) 以上述电池做电源,用上图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示):
_______________________________________________________,
_______________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com