
科目: 来源:不详 题型:单选题
| A.离子晶体的晶格能越大离子键越强 |
| B.阳离子的半径越大则可同时吸引的阴离子越多 |
| C.通常阴、阳离子的半径越小、电荷越大,该阴阳离子组成离子化合物的晶格能越大 |
| D.拆开1mol离子键所需的能量叫该离子晶体的晶格能 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.CaO中的离子键比MgO的弱 |
| B.甲醇的沸点比甲醛的沸点高 |
| C.HF、H2O的沸点比HCl、H2S的沸点高很多 |
D.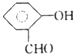 的沸点比的沸点高 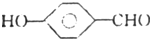 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B.熔点由高到低:Na>Mg>Al |
| C.硬度由大到小:金刚石>碳化硅>晶体硅 |
| D.晶格能由大到小:MgO>CaO>NaF>NaCl |
查看答案和解析>>
科目: 来源:不详 题型:单选题
A.由于NaCl 晶体和CsCl晶体中正负离子半径比(
| ||
| B.CaF2晶体中,Ca2+配位数为8,F-配位数为4不相等,主要是由于F-、Ca2+电荷(绝对值)不相同 | ||
| C.MgO的熔点比MgCl2高主要是因为MgO的晶体能比MgCl2大 | ||
| D.MCO3中M2+半径越大,MCO3热分解温度越低 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.①②③⑥ | B.①②④ | C.③⑤⑥⑦ | D.③⑤ |
查看答案和解析>>
科目: 来源:不详 题型:多选题
| A.含阳离子的化合物一定有阴离子 |
| B.晶格能由大到小:NaF>NaCl>NaBr>NaI |
| C.含有共价键的晶体一定具有高的熔、沸点及硬度 |
| D.空间利用率:面心立方>六方密堆积>体心立方 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B.熔点由高到低:Na>Mg>Al |
| C.硬度由大到小:金刚石>碳化硅>晶体硅 |
| D.晶格能由大到小:MgO>CaO>NaF>NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com