

科目: 来源: 题型:
已知180g葡萄糖(C6H12O6)完全燃烧时放热2804kJ太阳每分钟对地球表面辐射能量为2.1J/cm2;植物通过光合作用生成葡萄糖和氧气。设光合作用时太阳能量利用率10%,每片树叶面积以10cm2计算,这样的树叶100片要合成1.8g葡萄糖。问:
(1)需光照多长时间?
(2)若空气中含CO2质量分数为0.3%,需要标准状况下空气多少升?(标准状况下空气密度为1.29g/L)
(3)若标准状况下氧气密度为1.429g/L,问光合作用时除生成1.8g葡萄糖,还放出氧气多少升?
查看答案和解析>>
科目: 来源: 题型:
某不纯的烧碱样品中含有Na2CO3 3.8%、Na2O 5.8%、NaOH 90.4%。取M克样品,溶于质量分数为18.25%的盐酸溶液100g中,并用30%的NaOH溶液来中和剩余的盐酸至中性。把反应后的溶液蒸干后可得到固体质量是多少克?
查看答案和解析>>
科目: 来源: 题型:阅读理解
先阅读下列短文,再回答下列问题:
在酸性条件下,次氯酸钠(NaClO)、过氧化氢都有很强的氧化性,可将Fe2+氧化为Fe3+。Mg(OH)2和Fe(0H)3在溶液中生成时呈胶状物或絮状物沉淀,而MgCO3在水中煮沸可转变为Mg(OH)2。“卤块”的主要成分为MgCl2,还含有FeCl2、FeCl3、MnCl2等杂质。若以它为原料,按下图工艺流程即可制得“轻质氧化镁”。若要求产品不含杂质离子,而且成本较低,流程中所用试剂或pH控制可参考表1、表2来确定。
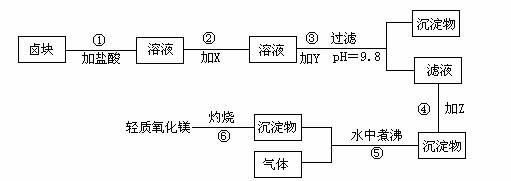
表1: 表2:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 2.7 | 3.7 |
| Fe(OH)3 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
| 工业品 | 规格 | 价格(元/吨) |
| 漂液 | 含NaClO 25.5% | 450 |
| 过氧化氢 | 含H2O2 30% | 240 |
| 烧碱 | 含NaOH 98% | 2100 |
| 纯碱 | 含Na2CO3 99.5% | 600 |
| 卤块 | 含MgCl2 30% | 310 |
请填下列空白:
(1)写出盐酸溶液中NaClO将FeCl2氧化成FeCl3,同时生成NaCl和H2O的化学方程式:
,写出在盐酸溶液中H2O2将FeCl2氧化成FeCl3,同时生成H2O的化学方程式: 。
(2)在步骤2中加入物质X,最佳的选择应是 ,理由是
。
(3)在步骤3中加入的物质应是 ,之所以要控制pH=9.8,其目的是
。
(4)在步骤4中加入物质应是 。
(5)在步骤5中发生的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
李同学在探究铁生锈的条件时,将铁钉浸没在试管里的食盐水中,一段时间后,发现试管底部出现了黑色粉末。李同学对此黑色粉末的组成做了如下几种猜测:
①Fe ②Fe2O3 ③Fe3O4 ④FeCl3 ⑤数种物质的混合物。请回答下列问题:
(1)你认为李同学的上述猜想中,不做实验就可排除的是 和 (填序号),理由是 ;你认为黑色粉末还可能是 ,理由是 。
(2)李同学将黑色粉末干燥后,用磁铁靠近,发现粉末能被磁铁吸引,于是得出结论:黑色粉末一定是铁粉。你认为李同学的结论对吗? ,理由是 。
查看答案和解析>>
科目: 来源: 题型:
欲在室温和1.01×105Pa条件下测定镁的相对分子质量,请利用下图给定的仪器(盛放镁条的隔板有小孔)组装成一套实验装置(每种仪器只允许用一次)。请回答下列问题:
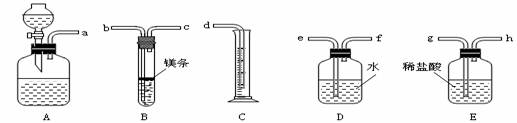
(1)装置A中的分液漏斗中盛放的液体是 ,其作用是
(2)假设气流方向由左向右,则各仪器的接口连接的先后顺序为(填小字母) ;
(3)连接好仪器后,要进行的操作有以下几步:①待仪器B中的物质恢复到室温时,测得量筒C中水的体积(若假设将测定的体积换算为标准状况下为VmL);②擦掉镁条表面的氧化膜,将其置于天平上称量(假定其质量为mg),并将其投入试管B中;③检查各装置的气密性;④旋开仪器A上分液漏斗的活塞,当镁条完全溶解时再关闭活塞。上述几步操作的先后顺序为 ;
(4)若未将试管B冷却至室温就测量量筒C中水的体积,这将会使所得镁的相对原子质量数据(选填“偏高”或“偏低”或“无影响”) ;
(5)若未擦净镁条表面氧化膜就进行实验,这将会使所测镁的相对原子质量数据(选填“偏高”或“偏低”或“无影响”) 。
查看答案和解析>>
科目: 来源: 题型:
密陀僧是一氧化铅,它可与碳反应:2PbO+C ![]() 2Pb + CO2↑、PbO+C
2Pb + CO2↑、PbO+C ![]() Pb + CO,有同学设计一简便实验以证明密陀僧中含有氧元素,在实验前后及过程中均通入氮气,试回答:(1)为了使实验成功,混合物中碳的含量应 (填“较多”或“较少”),原因是 ;
Pb + CO,有同学设计一简便实验以证明密陀僧中含有氧元素,在实验前后及过程中均通入氮气,试回答:(1)为了使实验成功,混合物中碳的含量应 (填“较多”或“较少”),原因是 ;
(2)该实验以干燥的氮气代替空气作为反应环境,其原因是 ;
(3)为了证明密陀僧中含有氧元素,应进行的操作是 。
查看答案和解析>>
科目: 来源: 题型:
为了确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。已知氧化铁和铝在高温下反应生成氧化铝和铁;铝和氢氧化钠的水溶液反应生成偏铝酸钠(NaAlO2)和氢气。
(1)若取ag样品,向其中加入足量的氢氧化钠溶液,测得生成的气体为bg。反应的化学方程式为 ,样品中铝的质量为 g;
(2)若取ag样品,使其在高温下恰好完全反应,该反应的化学方程式为
,样品中氧化铁与铝的质量比为 ;
(3)待(2)中反应产物冷却后,往其中加入足量的盐酸,测得生成的气体质量为cg,则该气体与(1)中所得的气体的质量比c∶b= 。
查看答案和解析>>
科目: 来源: 题型:
腌制食品中含有亚硝酸盐,它会影响健康及诱发癌症,但维生素C对亚硝酸盐的形成有阻挡作用。有一种设想:在含有亚硝酸盐(NaNO2)的腌制食品中加入过量的化肥氯化铵与其共热,生成无毒害的氮气、水、和氯化钠,过量氯化铵在持续加热的情况下分解为氨气与氯化氢挥发,此时腌制食品便可以放心食用。
(1)写出这种设想中反应的化学方程式 ;
(2)评价这种方案,并申述理由:
(3)请提出一条减少食用腌制食品中亚硝酸盐含量的措施: 。
查看答案和解析>>
科目: 来源: 题型:
亚硫酸钠(Na2SO3)受热会分解,它在有H2O存在时容易被空气中的氧气氧化为硫酸钠(Na2SO4)。实验室贮存亚硫酸钠的试剂瓶极易炸裂,你推测其原因可能是:
① ;② ;
如果试剂瓶在冬天容易炸裂,应是原因 (填上述的序号);如果试剂瓶在夏天容易炸裂,应是原因 。
查看答案和解析>>
科目: 来源: 题型:
向一盛有无色溶液的试管中加入另一种无色溶液,生成了一种白色沉淀。试根据你学过的酸、碱、盐的知识和题目要求,推测生成的白色沉淀和对应的两种无色溶液各是什么。
(1)推测一:如果沉淀不溶于稀硝酸,沉淀可能是 ,两种无色溶液中的溶质分别是 ;
(2)推测二:如果白色沉淀溶于稀硝酸且有气体产生,沉淀可能是 ,两种无色溶液中的溶质分别是 ;
(3)推测三:如果白色沉淀溶于稀硝酸但不产生气体,沉淀可能是 ,两种无色溶液中的溶质分别是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com