

科目: 来源: 题型:
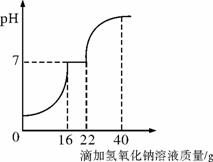
在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是因为里面含有氯化铁。为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小霞做了如下实验:取20 g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如下图所示的关系。
求该工业盐酸中氯化铁的溶质质量分数。(结果保留至0.1%)
查看答案和解析>>
科目: 来源: 题型:
我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品。为了测定样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来讲行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石 样品质量/g | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸 的质量/g | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体 的质量/g | 6.0 | 4.0 | 1.0 | 1.0 |
试回答:
(1)10.0 g样品与45 g盐酸充分反应后,盐酸是否还剩余________(填“是”或“否”),样品中碳酸钙的质量分数是________。
(2)10.0 g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程,计算结果精确到小数点后两位)
查看答案和解析>>
科目: 来源: 题型:
某兴趣小组从废铝锅底部剪一块铝片,将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如下图(假设酸与氧化膜反应时没有H2产生,其他杂质不与酸反应)。请回答:
(1)从图中看出,该反应产生了H2________g。
(2)产生氢气的化学方程式为:________________________________________________________________________;铝片中铝单质的质量为________g。
(3)求被氧化的铝的质量占未氧化时铝片总质量的质量分数,写出计算过程。

查看答案和解析>>
科目: 来源: 题型:
小明同学在某化工厂进行社会实践,技术员与小明一起分析由氯化钙和氯化钠组成的产品中氯化钠的含量。现取13.4 g固体样品,全部溶于96.6 g水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如下图所示的曲线关系。
技术员提示小明:氯化钙与碳酸钠反应的化学方程式:CaCl2+Na2CO3===CaCO3↓+2NaCl。求:
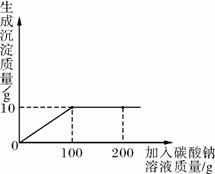
(1)当加入200 g碳酸钠溶液时,溶液中的溶质是______________________。
(2)当氯化钙与碳酸钠恰好完全反应时,过滤,所得溶液中溶质的质量分数是多少?(请写出必要的解题过程)
查看答案和解析>>
科目: 来源: 题型:
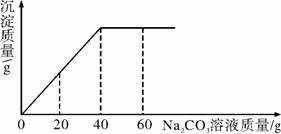
实验室有一瓶未知浓度的BaCl2溶液,某同学取出150 g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如下图所示。已知:BaCl2+Na2CO3===BaCO3↓+2NaCl。请计算:
(1)配制26.5%的Na2CO3溶液80 g,需要Na2CO3固体__________g。
(2)BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)
查看答案和解析>>
科目: 来源: 题型:
某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,实验测得相关数据如下图所示:

(1)剩余的混合物中二氧化锰的质量为____g,反应生成氧气的质量为____g。
(2)计算该过氧化氢溶液中溶质质量分数。
(3)实验表明硫酸铜溶液在该反应中也能起到二氧化锰的作用。若用5.6 g无水硫酸铜代替二氧化锰进行本实验,计算剩余的溶液中溶质的质量分数。(硫酸铜全部溶于水,计算时保留到0.1%)
查看答案和解析>>
科目: 来源: 题型:
请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:
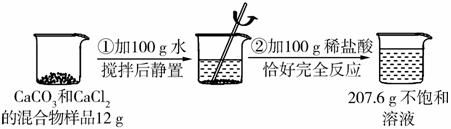
(1)实验所用稀盐酸溶质的质量分数为___________。
(2)计算原混合物样品中CaCl2的质量(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
某校化学小组的同学想探究生铁中碳的含量,他们取组成完全相同的三份生铁(假设生铁中只含铁和碳),分别加入50 g稀硫酸中进行实验(实验Ⅰ、Ⅱ、Ⅲ),充分反应后得到下表的实验数据:
| 实验次数 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 生铁的质量/g | 2.9 | 5.8 | 7.2 |
| 氢气的质量/g | 0.1 | 0.2 | 0.2 |
请计算:(计算结果精确到0.1%)
(1)该生铁中碳的质量分数为________。
(2)所用稀硫酸的溶质质量分数是多少?
查看答案和解析>>
科目: 来源: 题型:
工业上用电解NaCl溶液的方法来制取NaOH、Cl2和H2,反应的化学方程式为:2NaCl+2H2O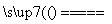 2NaOH+H2↑+Cl2↑。现取一定质量分数的NaCl溶液214.6 g进行电解,当NaCl完全反应时,生成0.4 g H2。
2NaOH+H2↑+Cl2↑。现取一定质量分数的NaCl溶液214.6 g进行电解,当NaCl完全反应时,生成0.4 g H2。
(1)当NaCl完全反应时,生成Cl2的质量为______g,参加反应的NaCl的质量为________g。
(2)当NaCl完全反应时,所得NaOH溶液中溶质的质量分数为多少?(假设生成的Cl2和H2全部逸出)
查看答案和解析>>
科目: 来源: 题型:
为测定某石灰石样品中碳酸钙的含量,取10.0 g于烧杯中,再向其中加入稀盐酸50.0 g,恰好完全反应(杂质不反应),反应后烧杯中物质的总质量为56.7 g。
(1)生成CO2的质量为________。
(2)求石灰石样品中碳酸钙的质量分数(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com