

科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:选择题
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想,其中一定不成立的是
A.Mg(NO2)2、NO2、O2 B.MgO、NO2、O2
C.Mg3N2、O2 D.MgO、NO2、N2
查看答案和解析>>
科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:选择题
“类推”是一种在化学学习中常用的方法,下列类推结论中正确的是
A.ⅣA族元素氢化物熔点顺序:GeH4>SiH4>CH4;则ⅥA族元素氢化物熔点顺序也应为:H2Se>H2S>H2O
B.第2周期元素氢化物的稳定性顺序是HF>H2O>NH3;则第3周期元素氢化物的稳定性顺序也是HCl>H2S>PH3
C.工业上用电解熔融的氯化镁制备镁单质,工业上也可用电解熔融的氯化铝制备铝单质
D.BaCl2溶液中通入SO2无沉淀产生,则Ba(NO3)2溶液中通入SO2也无沉淀产生
查看答案和解析>>
科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:选择题
为了探索外界条件对反应aX(g)+bY(g) cZ(g)的影响,以X和Y物质的量之比为a∶b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如下图所示。
cZ(g)的影响,以X和Y物质的量之比为a∶b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如下图所示。
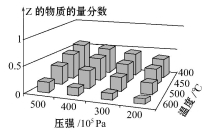
下列判断正确的是
A.ΔH>0 a+b>c B.ΔH<0 a+b<c
C.ΔH<0 a+b>c D.ΔH>0 a+b<c
查看答案和解析>>
科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:选择题
如图装置中,在U形管底部盛有CCl4,分别在U形管两端小心倒入饱和食盐水和稀硫酸溶液,并使a、b两处液面相平,然后分别塞上插有生铁丝的塞子,密封好,放置一段时间后,下列有关叙述中错误的是
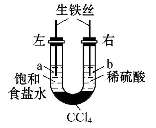
A.铁丝在两处的腐蚀速率:a < b
B.a、b两处相同的电极反应式为Fe-2e-==Fe2+
C.一段时间后,a处液面高于b处液面
D.生铁丝中的碳在a、b两处分别作原电池的负极和正极
查看答案和解析>>
科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:选择题
电导率可用于衡量电解质溶液导电能力的大小。室温下,用0.100 mol·L-1 NH3·H2O滴定10 mL浓度均为0.100 mol·L-1HCl和CH3COOH的混合液,电导率曲线如图所示。
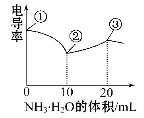
下列说法正确的是
A.①溶液中c(H+)为0.200 mol·L-1
B.溶液温度高低为①>③>②
C.③点溶液中有c(Cl—)>c(CH3COO—)
D.③点后因离子数目减少使电导率略降低
查看答案和解析>>
科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:选择题
根据下图海水综合利用的工业流程图,判断下列说法正确的是
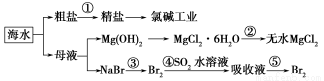
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2
C.从能量角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程
D.从第③步到第⑤步的目的是为了浓缩富集溴
查看答案和解析>>
科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:填空题
(17分)Na、Cu、Al、O、C、H是常见的六种元素。
(1)Al位于元素周期表第_____周期第_____族;Cu的基态原子价电子排布式为__________。
(2)用“>”或“<”填空:
第一电离能 | 离子半径 | 沸点 |
Na_______Al | O2—_______Na+ | CH4______H2O |
(3)250℃时,以镍合金为催化剂,向4 L容器中通入6 mol CO2、6 mol CH4,发生如下反应:CO2 (g)+CH4(g)  2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
物 质 | CH4 | CO2 | CO | H2 |
体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
①此温度下该反应的平衡常数K=__________
②已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= 890.3 kJ·mol-1
890.3 kJ·mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g) △H=+2.8 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H= 566.0 kJ·mol-1
566.0 kJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) 的△H=________________
2CO(g)+2H2(g) 的△H=________________
(4)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如右图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是_____________________.
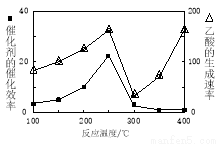
②为了提高该反应中CH4的转化率,可以采取的措施是__________________
(5)利用高温电解技术可将释放的CO2转化为具有工业利用价值的产品。
反应方程式为: ,其工作原理示意图如下:
,其工作原理示意图如下:
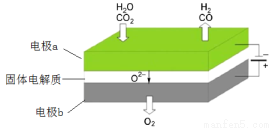
CO2在电极a放电的反应式是_______________________________
查看答案和解析>>
科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:填空题
(13分)6-羰基庚酸是一种重要的化工中间体,其合成路线如下:

已知: 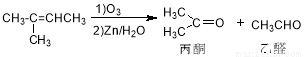
(1)反应①的条件是 ,C→D的反应类型是 ,C中官能团的名称是 。
(2)下列说法中正确的是
a.C能被催化氧化成酮
b.D不能使酸性高锰酸钾溶液褪色
c.Ni催化下1mol E最多可与2molH2加成
d.G既能发生取代反应,又能发生加成反应
(3)E与新制Cu(OH)2反应的化学方程式为 。
(4)G的同分异构体有多种。请写出三种结构中含有 、且属于酯类的同分异构体: 、 、
、且属于酯类的同分异构体: 、 、
。
(5)已知“Diels-Alder反应”为: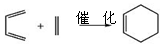 。物质D与呋喃(
。物质D与呋喃(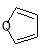 )也可以发生“Diels-Alder反应”,该化学反应方程式为: 。
)也可以发生“Diels-Alder反应”,该化学反应方程式为: 。
查看答案和解析>>
科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:填空题
(8分)SO2、NO是大气污染物。工业上吸收SO2 和NO,同时获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
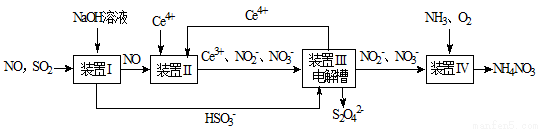
(1)装置Ⅰ中生成HSO3-的离子方程式为 ;
(2)向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: ;
(3)装置Ⅲ中,电解槽的阳极发生的电极反应为 ;
(4)从装置Ⅳ中获得粗产品NH4NO3的实验操作依次为 、 、过滤、洗涤等。
查看答案和解析>>
科目: 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:填空题
(14分)亚硝酸盐是一种常见的食品添加剂,使用时必须严格控制其用量。为检测某食品中亚硝酸盐含量(通常以1kg样品中含NaNO2的质量计),某研究小组设计了如下两种实验方案:(提示 : 无色气体B遇空气显红棕色)
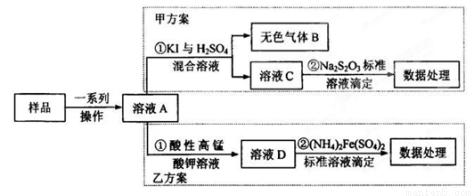
(1)甲方案②中常用 做指示剂。若需配制80 mL0.001 mol·L-1的Na2S2O3标准溶液。现给出下列仪器(配制过程中可能用到):①50 mL烧杯②胶头滴管③天平④80 mL容量瓶⑤100 mL容量瓶⑥玻璃棒,按使用仪器的先后顺序排列正确的是
A.③①⑤⑥② B.③①⑥④② C.③①⑥⑤② D.③①④⑥②
请写出配制Na2S2O3标准溶液时定容的操作
(2)已知酸性条件下MnO4—被还原为Mn2+,请写出乙方案①的离子方程式
(3)若取样品ag,按乙方案进行测定,准确量取12.00mL0.0005mol/L的酸性KMnO4溶液(过量)与溶液A反应。反应后溶液用0.0010mol/L(NH4)2Fe(SO4)2标准溶液滴定至溶液紫色刚好褪去;重复上述实验2次,平均消耗(NH4)2Fe(SO4)2溶液10.00mL.则1kg样品中 NaNO2的质量为_______mg.
(4)若乙方案②中使用的(NH4)2Fe(SO4)2溶液暴露在空气中时间过长,则会导致测定出的NaNO2含量 (填“偏高”、“偏低”或“不影响”)
(5)小组经过讨论,认为 方案更佳,原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com