
科目: 来源:2015-2016学年北京市东城区高二下学期期末化学试卷(解析版) 题型:选择题
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是( )
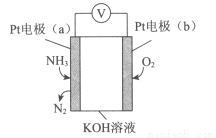
A.溶液中OH-向电极a移动
B.O2在电极b上发生还原反应
C.反应消耗的NH3与O2的物质的量之比为4:5
D.电极a的反应式为2NH3-6e-+6OH-=N2+6H2O
查看答案和解析>>
科目: 来源:2015-2016学年北京市东城区高二下学期期末化学试卷(解析版) 题型:选择题
向密闭容器中,按n(CO):n(H2)=1:2充入反应物,发生反应:CO(g)+2H2(g) CH3OH(g) △H<0。L(L1、L2)、X可分别代表压强或温度,下图表示L一定时,平衡混合物中CH3OH的体积分数随X的变化关系。
CH3OH(g) △H<0。L(L1、L2)、X可分别代表压强或温度,下图表示L一定时,平衡混合物中CH3OH的体积分数随X的变化关系。

下列说法中,正确的是( )
A.X代表压强 B.L1 <L2
C.平衡常数:K(A)=K(B) D.在C点时,CO转化率为75%
查看答案和解析>>
科目: 来源:2015-2016学年北京市东城区高二下学期期末化学试卷(解析版) 题型:填空题
25℃时,现有浓度均为0.10mol·L-1的两种溶液:①CH3COOH溶液、②NaOH溶液。请回答:
(1)溶液①的pH __________(填“>”“=”或“<”)1,原因是______________。
(2)将等体积①和②混合,所得溶液显__________(填“酸”“碱”或“中”)性,原因是__________________(用离子方程式表示)。
(3)向①中逐滴加入②至所得溶液pH=7的过程中(不含pH=7时的溶液),下列关系正确的是_________(填选项序号)。
a.c(H+)>c(OH-)
b.c(Na+)<c(CH3COO-)
C.c(Na+) =c(CH3COO-)+c(CH3COOH)
d.c(OH-) +c(CH3COO-) =c(H+) +c(Na+)
查看答案和解析>>
科目: 来源:2015-2016学年北京市东城区高二下学期期末化学试卷(解析版) 题型:填空题
用石墨电极电解饱和NaCl溶液的装置如下图所示:

请回答:
(1)电解饱和NaCl溶液的总反应方程式为______________。
(2)a端是直流电源的______________(填“负”或“正”)极。
(3)阳极上发生的反应式是__________________。
(4)结合电极反应式说明电解池右侧NaOH溶液浓度增大的原因是__________________。
查看答案和解析>>
科目: 来源:2015-2016学年北京市东城区高二下学期期末化学试卷(解析版) 题型:填空题
一定温度下,2L密闭容器中充入0.40 mol N2O4,发生反应:N2O4(g) 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
时间/s | 20 | 40 | 60 | 80 | 100 |
c(NO2 )/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
请回答:
(1)20 s内,v(NO2)=____________mol·L-1·s-1。
(2)升高温度时,气体颜色加深,则正反应是____________(填“放热”或“吸热”)反应。
(3)该温度下反应的化学平衡常数数值为_____________。
(4)相同温度下,若开始时向该容器中充入的是0.20 molN2O4和0.40molNO2,则达到平衡后,c(NO2)=_____________。
查看答案和解析>>
科目: 来源:2015-2016学年北京市东城区高二下学期期末化学试卷(解析版) 题型:实验题
某研究小组以银盐为实验对象,研究难溶盐时进行了如下实验:
①0.1 mol·L-1 AgNO3溶液和0.1 mol·L-1 NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;
②向滤液b中滴加0.1 mol·L-1KI溶液,出现浑浊;
③向沉淀c中滴加0.1 mol·L-1KI溶液,沉淀变为黄色;
④向AgI中滴加0.1 mol·L-l NaCl溶液,无明显现象。
已知:25℃时,AgCl和AgI的溶解度分别是1.5×10-4 g和3×10-7 g
请回答:
(1)沉淀c是__________。
(2)步骤②中的现象说明滤液b中含有的微粒是_________。
(3)步骤③中反应的离子方程式是__________。
(4)根据实验,可以得出的结论是___________。
查看答案和解析>>
科目: 来源:2015-2016学年北京市东城区高二下学期期末化学试卷(解析版) 题型:填空题
硼酸(H3BO3)为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能,提高机械强度,缩短熔融时间。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、Al2O3和SiO2等)为原料制备硼酸的工艺流程如下(部分操作和条件略):
I.向铁硼矿粉中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量双氧水,再调节溶液的pH约为5;
Ⅲ.过滤,将所得滤液蒸发浓缩、冷却结晶、过滤得粗硼酸和含镁盐的母液;
Ⅳ.粗硼酸精制得硼酸。
已知:生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 | |
开始沉淀时 | 3.8 | 5.8 | 2.2 | 10.6 |
完全沉淀时 | 4.7 | 8.3 | 4.0 | 12 |
注:金属离子的起始浓度为0.01 mol·L-1
请回答:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式:___________。
(2)为提高步骤I中的反应速率,可采取的措施有_________________(写出两条)。
(3)步骤Ⅱ的目的是_______________________。
(4)“粗硼酸”中的主要杂质是 ___________________。
查看答案和解析>>
科目: 来源:2015-2016学年北京市东城区高二下学期期末化学试卷(解析版) 题型:填空题
二氧化硫是一种重要的化工原料,主要用于生产硫酸、亚硫酸盐等。请回答:
(1)已知2SO2(g)+O2(g) 2SO3(g)是工业制硫酸的关键反应。下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
2SO3(g)是工业制硫酸的关键反应。下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
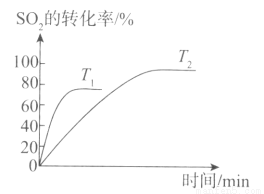
①T1__________(填“>”“<”或“=”)T2,判断的依据是_____________________;该反应为____________(填“放”或“吸”)热反应,判断的依据是___________________。
②下表为一定温度和压强下,4种投料比[n(SO2):n(O2)]分别为2:18、4:15、7:11和8:10时SO2的平衡转化率。
投料比 | a | b | c | d |
SO2平衡转化率/% | 97.1 | 96.8 | 95.8 | 90.0 |
i.b对应的投料比为_____________。
ii.投料比为8:10时,平衡混合气体中SO3体积分数为_________________。
(2)钠碱循环法吸收硫酸厂尾气中的SO2并将其转化为硫酸的工艺如下:

①吸收池中发生反应的离子方程式是_____________________。
②电解池的构造示意图如下:
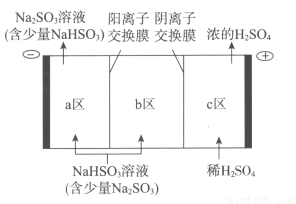
i.在图中标示出b区的Na+和HSO3-的移动方向。
ii.请结合生成H2SO4的电极反应式说明c区除得到浓的硫酸外,还会得到什么物质:__________________。
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高一下质检化学试卷(解析版) 题型:选择题
自然环境与人们的生活息息相关。下列有关环境问题的说法不正确的是( )
A.氟利昂(CCl2F2)因破坏大气臭氧层而导致“温室效应”
B.将垃圾分类并回收利用是垃圾处理的发展方向
C.废旧电池的回收,其主要目的是保护环境,而不是回收金属
D.淀粉餐具被认为是有发展前景的一次性餐具,可有利于保护环境
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高一下质检化学试卷(解析版) 题型:选择题
下述实验操作正确或能达到预期目的的是( )

A.甲图:向容量瓶中转移溶液 B.乙图:实验室制取乙酸乙酯
C.丙图:实验室制备NH3 D.丁图:实验室制备氢氧化铁胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com