
科目: 来源:2017届广东省等四校高三上学期第一次联考化学试卷(解析版) 题型:实验题
铜的氯化物是重要的化工原料,广泛地用作有机合成催化剂。实验室中以粗铜(含杂质Fe)为原料,某种制备铜的氯化物的流程如下。

按要求回答下列问题:
(1)在进行操作①之前,要确认溶液中杂质已经完全沉淀,检验的具体操作和现象是 。
(2)上述流程中,所得固体1需要加稀盐酸溶解,其理由是
(3)溶液1可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)__________。
a.NaHCO3 b.NH3·H2O c.CuO d.Cu2(OH)2CO3
(4)现用如图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。

①按气流方向连接各仪器接口顺序是:a→ 、 → 、 →f、g→ 。
②为了防止生成氧化铜,实验时在大试管加热前要进行一步重要操作,其操作是 。
③实验过程中,饱和食盐水中出现少许浑浊的现象,请用化学相关原理和知识解释原因: 。
查看答案和解析>>
科目: 来源:2017届广东省等四校高三上学期第一次联考化学试卷(解析版) 题型:实验题
碱式氯化铝[ Al2(OH)nCl6-n ] 是利用工业铝灰和活性铝矾土为原料(主要含Al、Al2O3、SiO2及铁的氧化物)经过精制加工而成,此产品活性较高,对工业污水具有较好的净化效果。其制备流程如下:
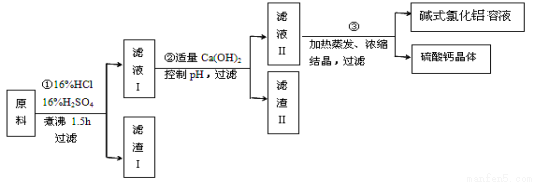
(1)原料需要粉碎,其目的是 ;滤渣I的主要成分是 ;
(2)步骤①在煮沸过程中,溶液逐渐变为浅绿色,检验溶液中呈浅绿色的阳离子常采用加入_________溶液进行检验(填试剂化学式)。
(3)步骤②中加入适量的Ca(OH)2并控制pH,其目的:一是生成碱式氯化铝;二是 ;已知碱式氯化铝的分散质粒子大小在1~100 nm之间,则区别滤液I与碱式氯化铝两种液体的物理方法是 ;若Ca(OH)2溶液过量,则步骤③得到的碱式氯化铝产率偏低,用离子方程式解释其原因为 ;
(4)某温度下若0.1 mol AlCl3溶于蒸馏水,当有2.5%水解生成Al(OH)3胶体时,吸收热量Q kJ ,该水解过程的热化学反应方程为 。
查看答案和解析>>
科目: 来源:2017届广东省等四校高三上学期第一次联考化学试卷(解析版) 题型:填空题
“金属钙线”是炼制优质钢材的脱氧脱磷剂,某“金属钙线”的主要成分为金属Fe和金属钙Ca,并含有3.5%(质量分数)CaO。
(1)Ca的原子结构示意图为 。其最高价氧化物对应水化物的碱性比Mg(OH)2 (填“强”或“弱”)。
(2)Ca与非金属性最强的元素A形成化合物D,写出D的电子式 。
(3)配平用“金属钙线”脱氧脱磷的方程式:

(4)将“金属钙线”溶于稀盐酸后,再滴加双氧水发生的离子方程式是 。
(5)取3.2 g“金属钙线”试样,与水充分反应生成448 mL H2(标准状况),在所得溶液中通入适量CO2,最多能得到CaCO3 g(取两位有效数字)。
查看答案和解析>>
科目: 来源:2017届广东省等四校高三上学期第一次联考化学试卷(解析版) 题型:填空题
铁、钴(Co)、镍(Ni)是同族元素,都是较活泼的金属,它们的化合物在工业上有重要的应用.
(1)草酸钴(CoC₂O?)是一种难溶于水的浅粉红色粉末,通常用硫酸钴溶液和草酸铵溶液反应制得,写出该反应的离子方程式:
(2)现将含0.5molFeCl3的溶液和含0.5molKSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3++SCN-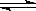 Fe(SCN)2+(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图1所示:则该反应△H 0(填“>”或“<”),温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45mol /L,求达到平衡时的平均反应速率v(SCN-)= mol·L-1·S-1 ,该温度下的Fe3+的平衡转化率为 ,该温度下反应的平衡常数为 。
Fe(SCN)2+(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图1所示:则该反应△H 0(填“>”或“<”),温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45mol /L,求达到平衡时的平均反应速率v(SCN-)= mol·L-1·S-1 ,该温度下的Fe3+的平衡转化率为 ,该温度下反应的平衡常数为 。

(3)已知某溶液中,Co2+、Ni2+的浓度分别为0.60mol/L和1.2mol/L,取一定量的该溶液,向其中滴加NaOH溶液,当Co(OH)2开始沉淀时,溶液中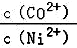 的值等于 .(取两位有效数字)(已知Ksp[Co(OH)2]=6.0×10﹣15,Ksp[Ni(OH)2]=2.0×10﹣15)
的值等于 .(取两位有效数字)(已知Ksp[Co(OH)2]=6.0×10﹣15,Ksp[Ni(OH)2]=2.0×10﹣15)
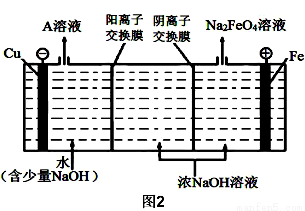
(4)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图2所示,则阳极的电极反应式为 。
查看答案和解析>>
科目: 来源:2017届河北省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列有关焰色反应的叙述正确的是( )
A.只有金属的化合物灼烧时才会有不同的颜色
B.每次实验后,铂丝都要用水洗净
C.若透过蓝色钴玻璃只看到紫色,说明样品中含钾元素而一定不含钠元素
D.若样品灼烧呈黄色,判断一定有钠元素,但不能排除含其他金属元素
查看答案和解析>>
科目: 来源:2017届河北省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列用品的有效成分及用途对应错误的是( )
A.用品: 有效成分:NaCl用途:做调味品
有效成分:NaCl用途:做调味品
B.用品: 有效成分:Na2CO3用途:做发酵粉
有效成分:Na2CO3用途:做发酵粉
C.用品: 有效成分:Al(OH)3用途:做抗酸药
有效成分:Al(OH)3用途:做抗酸药
D.用品: 有效成分:Ca(ClO)2用途:做消毒剂
有效成分:Ca(ClO)2用途:做消毒剂
查看答案和解析>>
科目: 来源:2017届河北省高三上学期第一次月考化学试卷(解析版) 题型:选择题
氢氧化铝可作为治疗胃酸过多的内服药,这是利用了氢氧化铝的( )
A.酸性 B.碱性 C.两性 D.氧化性
查看答案和解析>>
科目: 来源:2017届河北省高三上学期第一次月考化学试卷(解析版) 题型:选择题
等质量的钠进行下列实验,其中生成氢气最多的是( )
A.将钠投入到足量水中
B.将钠用铝箔包好并刺一些小孔,再放入足量的水中
C.将钠放入足量稀硫酸中
D.将钠放入足量稀盐酸中
查看答案和解析>>
科目: 来源:2017届河北省高三上学期第一次月考化学试卷(解析版) 题型:选择题
铝在空气中能够稳定存在的原因是( )
A.铝的活泼性差 B.铝的还原性差
C.铝与氧气不反应 D.铝表面有致密的氧化膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com