
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.水库中的钢闸门通常连接锌块,是采用了牺牲阳极的阴极保护法
B.化学电源都是一次能源
C.铁的表面镀铜的过程中,铜极连接电源负极
D.合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其组成成分金属强
查看答案和解析>>
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.需要加热的反应说明它是吸热反应
B.已知C(石墨,s)===C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol,若将含0.6 mol H2SO4的稀硫酸与含1 mol NaOH的稀溶液混合,放出的热量等于57.3 kJ
D.已知2C(s)+2O2(g)===2CO2(g) ΔH1;2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1>ΔH2
查看答案和解析>>
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
已知热化学方程式:2SO2(g)+ O2(g)  2 SO3(g) △ H = ―198kJ/mol,下列说法正确的是( )
2 SO3(g) △ H = ―198kJ/mol,下列说法正确的是( )
A.2 L SO3气体分解成1 L O2与2 L SO2吸收198 kJ热量
B.1 mol O2与2 mol SO2混合,生成气态SO3放出的热量等于198 kJ
C .1个O2分子与2个SO2分子反应生成2个SO3气体分子放出198 kJ热量
D.在相同条件下,1 mol O2与2 mol SO2的能量总和大于2 mol SO3气体的能量
查看答案和解析>>
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
已知化学反应A2(g)+B2(g)== 2AB(g)的能量变化如图所示,则下列叙述中正确的是:( )
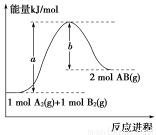
A.该反应的反应热ΔH=+(a-b)kJ/mol
B.每生成2分子AB吸收b kJ热量
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量
查看答案和解析>>
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
如图所示,铜片、锌片和石墨棒用导线连接后插入番茄里,电流计中有电流通过,则下列说法正确的是( )
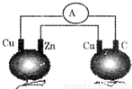
A.石墨是阴极 B.两个铜片上都发生氧化反应
C.两个番茄都形成原电池 D.锌片是负极
查看答案和解析>>
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
有关电化学知识的描述正确的是( )。
A.已知CaO+H2O===Ca(OH)2放出大量的热,故可把该反应设计成原电池
B.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁做负极、铜做正极
C.理论上说,任何能自发进行的氧化还原反应都可设计成原电池
D.某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag,装置中的盐桥内可以是含琼脂的KCl饱和溶液
查看答案和解析>>
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
根据以下三个热化学方程式:
2H2S(g)+3O2(g)==2SO2(g)+2H2O(l) ΔH=-Q1 kJ/mol
2H2S(g)+O2(g)==2S(s)+2H2O(l) ΔH=-Q2 kJ/mol;
2H2S(g)+O2(g)==2S(s)+2H2O(g) ΔH=-Q3 kJ/mol。
判断Q1、Q2、Q3三者关系正确的是:( )
A.Q3>Q2>Q1 B.Q1>Q3>Q2 C.Q1>Q2>Q3 D.Q2>Q1>Q3
查看答案和解析>>
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其保持平衡,然后向左侧烧杯中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(不考虑两球的浮力变化)( )
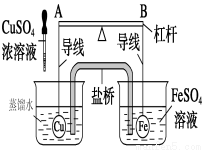
A.杠杆为导体或绝缘体时,均为A端高B端低
B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端高B端低
D.当杠杆为导体时,A端低B端高
查看答案和解析>>
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
某原电池装置如图所示。下列有关叙述中,正确的是( )

A.电池工作中,盐桥的中Cl-向负极移动
B.负极反应:2H++2e-===H2↑
C.工作一段时间后,两烧杯中溶液pH均不变
D.Fe作正极,发生氧化反应
查看答案和解析>>
科目: 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
298 K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是( )
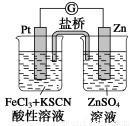
A.该原电池的正极反应是Zn-2e-=Zn2+
B.左侧烧杯中溶液的血红色逐渐褪去
C.该电池铂电极上有气泡出现
D.该电池总反应为3Zn+2Fe3+=2Fe+3Zn2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com