
科目: 来源: 题型:
(06年全国卷)(15分)在呼吸面具和潜水艇中可用过氧化钠作为供养剂。请选择适当的化学试剂和实验用品,用下图中的实验装置进行试验,证明过氧化钠可作供养剂。
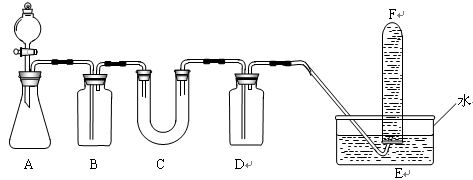
(1)A是制取CO2的装置。写出A中发生反应的化学方程式:_________________
(2)填写表中空格:(请在答题卡上填写)
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 |
|
C |
|
|
D |
|
|
(3)写出过氧化钠与二氧化碳反应的化学方程式:__________________________。
(4)试管F中收集满气体后,下一步实验操作是:__________________________。
查看答案和解析>>
科目: 来源: 题型:
(08山东临沂质检)下列叙述中正确的是( )
A. 第三周期元素的离子半径从左到右依次减小
B. HCl、PCl5、N2、CO2分子中所有原子都满足最外层8电子的结构
C. 晶体内可以不存在化学键,也可以同时存在离子键,极性键和非极性键
D. 若某离子化合物X2Y3中X3+和 Y2-的电子层结构相同, 则X、 Y两元素的原子序数之差可能是5、15或29
查看答案和解析>>
科目: 来源: 题型:
(06年全国卷)(9分)X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”):______________,理由是__________________________________________________;
(2)Y是___________,Z是___________,W是___________;
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8241。写出该化合物的名称及化学式是____________________。
查看答案和解析>>
科目: 来源: 题型:
(06年全国卷)由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol?L-1,c(SO42-)=0.8mol?L-1,则c(K+)为()
A. 0.15mol?L-1 B. 0.2mol?L-1 C . 0.3mol?L-1 D. 0.4mol?L-1
查看答案和解析>>
科目: 来源: 题型:
(08年广东卷)根据表1信息和,判断以下叙述正确的是 ()
表1 部分短周期元素的原子半径及主要化合价
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
|
|
|
|
|
|
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
查看答案和解析>>
科目: 来源: 题型:
![]() (06年全国卷)茉莉醛具有浓郁的茉莉花香,其结构简式所示,关于茉莉醛的下列叙述错误的是( )
(06年全国卷)茉莉醛具有浓郁的茉莉花香,其结构简式所示,关于茉莉醛的下列叙述错误的是( )
A . 在加热和催化剂作用下,能被氢气还原 B . 能被高锰酸钾酸性溶液氧化
C . 在一定条件下能与溴发生取代反应 D . 不能与氢溴酸发生加成反应
查看答案和解析>>
科目: 来源: 题型:
(06年重庆卷)X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是___________________________________。
(2)ZW2的电子式是_____________,它在常温下呈液态,形成晶体时,属于_________晶体。
(3)工业生产单质Y的原理是___________________________________________________(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是__________________________________________________________________________。
(5)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+ 和Br― 的物质的量之比是____________________________。
查看答案和解析>>
科目: 来源: 题型:
(07年山东卷)下列关于元素的叙述正确的是( )
A.金属元素与非金属元素能形成共价化合物
B.只有在原子中,质子数才与核外电子数相等
C.目前使用的元素周期表中,最长的周期含有36种元素
D.非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8
查看答案和解析>>
科目: 来源: 题型:
(06年重庆卷)X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是___________________________________。
(2)ZW2的电子式是_____________,它在常温下呈液态,形成晶体时,属于_________晶体。
(3)工业生产单质Y的原理是___________________________________________________(用化学方程式表示)。
(4)XY化学性质相似,则X与浓的NaOH溶液反应的化学方程式是__________________________________________________________________________。
(5)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+ 和Br― 的物质的量之比是____________________________。
查看答案和解析>>
科目: 来源: 题型:
(06年重庆卷)X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是___________________________________。
(2)ZW2的电子式是_____________,它在常温下呈液态,形成晶体时,属于_________晶体。
(3)工业生产单质Y的原理是___________________________________________________(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是__________________________________________________________________________。
(5)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+ 和Br― 的物质的量之比是____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com