
科目: 来源: 题型:
A.酚酞试液
B.氯化钡溶液
C.氢氧化钠溶液
D.硝酸银溶液
查看答案和解析>>
科目: 来源: 题型:
一种类似有机玻璃的塑料——聚丁烯酸甲酯有广泛的用途。合成这种有机塑料有不同的途径。以下合成途径副产品多为低污染或无污染物,原子利用率较高。因此较为符合“绿色化学”的要求。
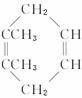
其反应过程是:
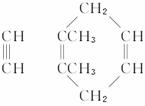
(1)写出图中化合物A、B、E的结构简式:A___________,B___________,E___________。
(2)在有机物反应中,加成类型的原子利用率最高。本反应过程中,属于此类反应特点的有______________________。
(3)写出下列反应的化学方程式:
①A→B:______________________________________;
②E→F:_______________________________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
四种盐在不同温度下的溶解度(g/100 g水)表
温度 溶解度 盐 | ||||||||
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | —① | — | — | — |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | — |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
①>
请回答:
(1)反应温度控制在30—35 ℃,是因为若高于35 ℃,则_______________,若低于30 ℃,则_________________;为控制此温度范围,采取的加热方法为_______________________。
(2)加料完毕后,继续保温30分钟,目的是____________________。静置后只析出NaHCO3晶体的原因是__________________。用蒸馏水洗涤NaHCO3晶体的目的是除去_______________杂质(以化学式表示)。
(3)过滤所得母液中含有_____________(以化学式表示),需加入_______________,并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl。
(4)测试纯碱产品中NaHCO3含水量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1—2滴酚酞指示剂,用物质的量浓度为c(mol·L-1)的HCl溶液滴定至溶液由红色到无色(指示![]() +H+
+H+![]()
![]() 反应的终点),所用HCl溶液体积为V1 mL,再加1—2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液总体积为V2mL。写出纯碱样品中NaHCO3质量分数的计算式:
反应的终点),所用HCl溶液体积为V1 mL,再加1—2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液总体积为V2mL。写出纯碱样品中NaHCO3质量分数的计算式:
NaHCO3(%)=___________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)该腐蚀属于电化腐蚀中的________腐蚀。
(2)正极的电极反应式是________________________________。
(3)用电极反应式、离子反应式、化学方程式表示锈的形成过程。________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)称取10.00 g样品,将其加入过量的NaOH浓溶液中共热并蒸干,AlN跟NaOH溶液反应生成NaAlO2,并放出氨气3.36 L(标准状况)。
①上述反应的化学方程式为_______________________________________________________。
②该样品中的AlN的质量分数为_____________。
(2)另取10.00 g样品置于反应器中,通入2.016 L(标准状况)O2,在高温下充分反应后测得气体的密度为1.14 g·L-1(已折算成标准状况,AlN不跟O2反应)。该样品中含杂质炭___________ g。
查看答案和解析>>
科目: 来源: 题型:
(1)用K2Cr2O7可以制备检验司机是否酒后开车的装置。现象是_______________________。
另一方面,铬对环境造成污染。其中,Cr(Ⅵ)的毒性比Cr(Ⅲ)毒性强200倍。制革厂排放的污染中约有1/3是有机物,其余是大量的含铬物质,直接排放污泥会对环境造成污染。1996年,外国科学家研究成功了一种技术,它较好地解决了制革厂废物利用与环境保护问题。工艺流程如下:
Ⅰ.污泥与普通黏土以一定比例混合(污泥占25%—30%)后制成砖坯,在窑中850—
Ⅱ.灼烧前期向窑中鼓入补充了氧气的空气。
Ⅲ.灼烧后期改用普通空气,且故意限制入窑空气的数量,使呈缺氧状态。烧制完成后,直到窑温降至
(2)前期鼓入富氧空气的原因是__________________________________________________。
(3)后期限制空气流入量的原因是_________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
第一步:金红石、炭粉混合,在高温条件下,通入Cl2制得TiCl4和一种可燃气体,该反应的化学方程式为_______________,该反应的还原剂是_____________________。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)写出此反应的化学方程式:____________________________________________________。
(2)简述从上述所得产物中获得金属钛的步骤。
____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
回答下列问题:
(1)这一实验证实了人们的一个猜想——鸽子高超的认路本领是由于( )
A.鸽子的眼力和对地形地貌极强的记忆力来判断方向
B.鸽子对地磁场的感应来判断方向
C.鸽子发射并接收反射回来的超声波来判别方向
D.鸽子发射并接收反射回来的次声波来判别方向
(2)科学家后来进一步解剖信鸽时,在信鸽的头部找到了许多某种物质的颗粒,该物质是( )
A.铁 B.氧化亚铁 C.三氧化二铁 D.四氧化三铁
查看答案和解析>>
科目: 来源: 题型:
(1)该两步反应的化学方程式分别是_____________________、_______________________。
(2)氮化硅薄膜材料是由硅烷与氨气在900 ℃到1 100 ℃温度下反应而制成的,其化学方程式为______________________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com