
科目: 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:选择题
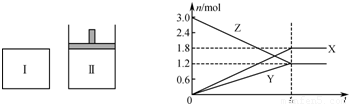
查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:解答题

查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:解答题
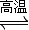 4CO(g)+SrS(s);△H=+akJ?mol-1
4CO(g)+SrS(s);△H=+akJ?mol-1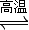 2CO2(g)+SrS(s);△H=+bkJ?mol-1
2CO2(g)+SrS(s);△H=+bkJ?mol-1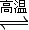 2CO(g)的△H=______kJ?mol-1.
2CO(g)的△H=______kJ?mol-1.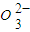 )=1.0×10-3mol/L,c(S
)=1.0×10-3mol/L,c(S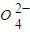 )=______mol/L.
)=______mol/L.查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:解答题
 +6H+═6Fe3++Cl-+3H2O
+6H+═6Fe3++Cl-+3H2O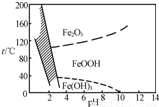
查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:解答题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2molSO2、1molO2 | 2molSO3 | mmolSO2、nmolO2、pmolSO3 |
| c(SO3)/mol?L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
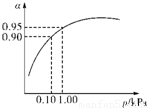
查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:解答题
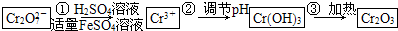
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
 与FeSO4溶液在酸性条件下反应的离子方程式______.
与FeSO4溶液在酸性条件下反应的离子方程式______.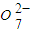 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.
查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:解答题
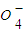 +______Fe2+═______Mn2++______Fe3++______H2O
+______Fe2+═______Mn2++______Fe3++______H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com