
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:选择题
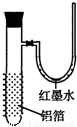
查看答案和解析>>
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:填空题
查看答案和解析>>
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:填空题
| 实验现象 | ⑦ | ③ | ||
| 实验结论 | ⑥ | ① |
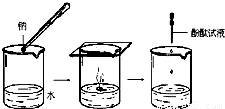
查看答案和解析>>
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:填空题
查看答案和解析>>
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:解答题
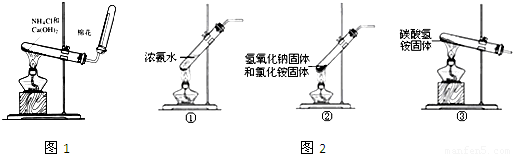
查看答案和解析>>
科目: 来源:2010-2011学年北京市东城区高一(上)期末化学试卷(解析版) 题型:解答题
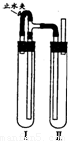
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com