

科目: 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:选择题
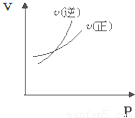
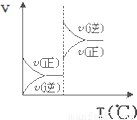
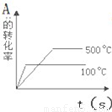
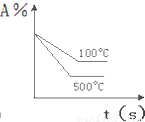
查看答案和解析>>
科目: 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:解答题
| 实验序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.20 |
查看答案和解析>>
科目: 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:解答题

查看答案和解析>>
科目: 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:解答题
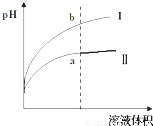
查看答案和解析>>
科目: 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:解答题
 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:| 温度°C | 450 | 500 | 550 | 600 |
| SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
查看答案和解析>>
科目: 来源:2008-2009学年浙江省宁波市高三(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com