
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:选择题
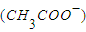 =c(Na+)时.该溶液一定呈中性
=c(Na+)时.该溶液一定呈中性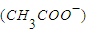 =c(Na+)时,醋酸与氢氧化钠恰好完全中和?
=c(Na+)时,醋酸与氢氧化钠恰好完全中和?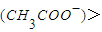 c(Na+)>c(H+)>c(OH-)时,不一定是醋酸过量
c(Na+)>c(H+)>c(OH-)时,不一定是醋酸过量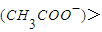 c(OH-)>c(H+)时,一定是氢氧化钠过量
c(OH-)>c(H+)时,一定是氢氧化钠过量查看答案和解析>>
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:选择题
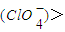 c
c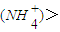 c(OH-)>?c(H+)?
c(OH-)>?c(H+)?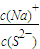 更接近2,可加入适量KOH
更接近2,可加入适量KOH查看答案和解析>>
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:选择题
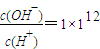 ,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:c(B+)>c(OH-)>c(H+)>c(A-)
,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:c(B+)>c(OH-)>c(H+)>c(A-)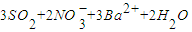 ═3BaSO4↓+2NO↑+4H+
═3BaSO4↓+2NO↑+4H+查看答案和解析>>
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:填空题
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
查看答案和解析>>
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:填空题

查看答案和解析>>
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:填空题
 ,经计算 (填”有”或”无”)Mg(OH)2沉淀生成.
,经计算 (填”有”或”无”)Mg(OH)2沉淀生成. 水解所致.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论).
水解所致.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论).
查看答案和解析>>
科目: 来源:2012-2013学年山西大学附中高二(上)期中化学试卷(理科)(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com