
科目: 来源: 题型:
【题目】变压吸附法的原理是利用分子筛吸附氮气和氧气能力的差异将二者进行分离。在吸附塔中,通过加压与减压的交替循环,可以使分子筛重复使用。部分过程的示意图如图:
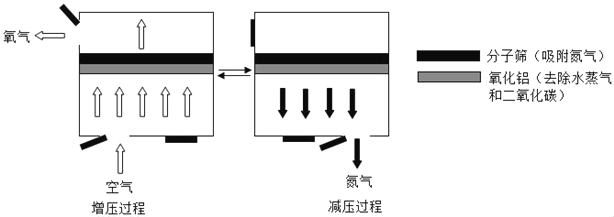
下列说法不正确的是( )
A. 变压吸法制取的氧气中含有稀有气体
B. 变压吸附法制取的氧气中含有二氧化碳
C. 分子筛对氮气的吸附能力与吸附塔内气体压强有关
D. 分子筛中发生的变化是物理变化
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室有一瓶过氧化氢溶液,标签如图。

试回答:
(1)实验室制取氧气时,通常要将30%的H2O2溶液稀释,其可能原因是_______。
(2)实验中需用6%的过氧化氢溶液100g,需30%的H2O2溶液体积为_____mL,加水为_________mL 。
(3)某同学取6.8g上述稀释后的溶液,用KMnO4溶液来测定其浓度,反应的化学方程式为2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+SO2↑+8H2O,恰好完全反应时消耗溶质KMnO4质量为0.632g,计算稀释后溶液的实际浓度_________(写出计算过程)。
(4)若溶液稀释过程是正确的,则实际浓度偏低的可能原因是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】小苏打和食盐是厨房中常用物质。现有一包白色固体,可能由NaHCO3和NaCl中的一种或两种组成。某科学小组同学展开了系列拓展性研究。
(一)定性分析:
(实验目的)确定白色固体的组成:
(实验方案)
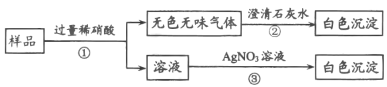
(实验结论)该白色固体由NaHCO3和NaCl两种物质组成。
(1)实验步骤①中选用稀硝酸而不用稀盐酸的原因是__________;
(2)实验步骤②中生成白色沉淀的化学反应方程式为__________。
(二)定量分析:
(实验目的)测定该白色固体中NaHCO3的质量分数:
(实验方案)用气体法测定样品中NaHCO3的质量分数。实验装置如下:
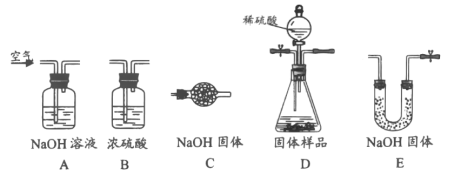
(1)用上述装置完成本实验,装置的连接顺序是A→____→C(填装置的字母编号,装置不重复使用)。
(2) D装置中发生反应的化学方程式为_______。
(3)如果没有经过A装置而直接通入空气,会使测量结果______(填“变大”、“变小”或“不变”)。
(4) C装置的作用是________。
(5) D装置中的反应完全后,称量前,还需要进行的实验操作是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚铜(CuCl)是一种难溶于水和乙醇,在潮湿空气中易变质,广泛应用于冶金、电镀、医药等行业的原料。CuCl的制备流程如下:
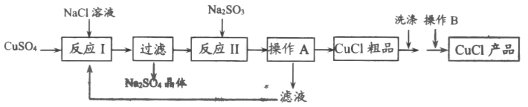
(1)“反应Ⅰ”中发生的化学方程式为_______。
(2)反应Ⅰ“过滤”后所得的滤液中,除了Cu2+, Na+, Cl-外,还存在较多的离子是_______(写离子符号)
(3)“反应Ⅱ”中发生的化学变化是2CuCl2+Na2SO3 +H2O =2CuCl↓+2NaCl+ H2SO4,其中化合价发生改变的元素有_______;反应过程中溶液的pH_______(选填“变大”、“变小”或“不变”)。
(4)本流程中可以循环利用的物质是_______。(写名称)
(5)在洗涤过程中用乙醇而不用水洗涤的原因是_______。
(6)“操作B”的名称是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】小华同学配制50g溶质质量分数为20%的NaCl溶液,操作流程如图:

(1)小华同学应称取的NaCl质量为________g。
(2)指出图中的一处错误:________。
(3)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应________。
A 增加适量氯化钠固体 B 减少适量氯化钠固体 C 调节平衡螺母
(4)在用量筒量取水的过程中,当液面接近刻度线时,他的操作如图所示,其中规范的是____(填序号)。
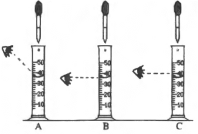
(5)如果小华配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有______(填序号)。
A 配制溶液的烧杯内壁湿润
B 称量纸上残留少量食盐
C 向烧杯中加水时,有少量水溅出烧杯外
查看答案和解析>>
科目: 来源: 题型:
【题目】下列为实验室常用的实验装置,回答问题:

(1)写出带有标号仪器的名称:①________;②____________。
(2)用锌和稀硫酸制取氢气,应选用的发生装置是___________(填序号,下同) ,收集装置是__________。
(3)实验室常用稀盐酸和石灰石反应制CO2,该反应的化学方程式__________;

(4)上图所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是_______,植物油上方原有的空气对实验结果_________(填“有”或“无”)明显影响。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为部分元素的粒子结构示意图。
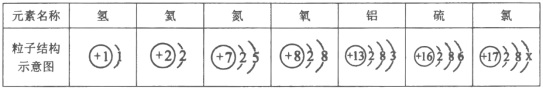
请回答下列问题:
(1)若氯原子最外层得到一个电子,其微粒符号为_______;
(2)表中具有相对稳定结构的原子是_______ (填元素符号);
(3)根据表中信息,确定一个硫化氢分子中所含电子总数为_______;
(4)将氮元素与铝元素形成的化合物放入水中,立即生成白色沉淀氢氧化铝,并放出一种有刺激性气味的气体。此反应的化学方程式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列反应事实写出相应的化学方程式。
(1)稀硫酸与锌粒反应制氢气:_________;
(2)用氨水中和工业废水中含有的稀硫酸:_________;
(3)硫酸铵与熟石灰研磨:_________;
(4)工业上用赤铁矿在高温下炼铁:_________;
(5)甲烷在足量氧气中充分燃烧:_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,其反应的化学方程式为: aC3H8O+bO2![]() cCO2+dH2O+eX,测得反应前后各物质的质量如下表:
cCO2+dH2O+eX,测得反应前后各物质的质量如下表:
物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 8.8 | x |
下列判断正确的是( )
A. 表中x的值为1.8B. x可能是该反应的催化剂
C. X可能为甲烷D. 方程式中a:b=1:4
查看答案和解析>>
科目: 来源: 题型:
【题目】往AgNO3和Cu(NO3)2的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤
渣中加入稀盐酸,有气泡产生。根据上述现象分析,你认为下面结论不正确的是( )
A. 滤渣的质量小于加入镁粉的质量B. 滤渣中一定有镁粉
C. 滤液中一定有Mg2+D. 滤液的颜色为无色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com